题目内容
(1)下列曲线分别表示元素某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质),把与下面的元素有关性质相符合的曲线的标号填入相应括号中.

①ⅡA族元素的最外层电子数
③O2-、F-、Na+、Mg2+、Al3+的离子半径
⑤第二周期元素Be、B、C、N、O的原子半径
(2)比较下列性质(用“>”、“=”、“<”填空)
①氧化性 Cl2
④稳定性 H2S
(3)元素性质呈周期性变化的决定因素是
A.元素原子半径大小呈周期性变化 B.元素的相对原子质量依次递增
C.元素原子核外电子排布呈周期性变化 D.元素的最高正化合价呈周期性变化.

①ⅡA族元素的最外层电子数
a
a
②ⅦA族元素氢化物的沸点c
c
③O2-、F-、Na+、Mg2+、Al3+的离子半径
b
b
④第三周期元素的最高化合价e
e
⑤第二周期元素Be、B、C、N、O的原子半径
b
b
(2)比较下列性质(用“>”、“=”、“<”填空)
①氧化性 Cl2
>
>
Br2 ②酸性 H3PO4<
<
H2SO4 ③碱性 Mg(OH)2>
>
Al(OH)3④稳定性 H2S
<
<
H2O ⑤还原性H2S>
>
HCl(3)元素性质呈周期性变化的决定因素是
C
C
.A.元素原子半径大小呈周期性变化 B.元素的相对原子质量依次递增
C.元素原子核外电子排布呈周期性变化 D.元素的最高正化合价呈周期性变化.
分析:(1)①同主族元素的原子最外层电子数相同;
②同主族元素的氢化物的沸点从上到下逐渐升高(有氢键的除外);
③电子层越多微粒半径越大,电子层一样,则核电荷数越多半径越小;
④同周期元素的最高化合价从左到右逐渐升高;
⑤周期元素的原子半径从左到右依次减小;
(2)①同主族元素的单质的氧化性从上到下逐渐减弱;
②同周期元素的最高价氧化物对应水化物的酸性从左到右逐渐增强;
③同周期元素的最高价氧化物对应水化物的碱性从左到右逐渐减弱;
④同主族元素的氢化物的稳定性从上到下逐渐减弱;
⑤同周期元素的单质的氧化性从左到右逐渐增强,离子的还原性逐渐减弱.
(3)元素性质呈周期性变化的决定因素是元素原子核外电子排布呈周期性变化.
②同主族元素的氢化物的沸点从上到下逐渐升高(有氢键的除外);
③电子层越多微粒半径越大,电子层一样,则核电荷数越多半径越小;
④同周期元素的最高化合价从左到右逐渐升高;
⑤周期元素的原子半径从左到右依次减小;
(2)①同主族元素的单质的氧化性从上到下逐渐减弱;
②同周期元素的最高价氧化物对应水化物的酸性从左到右逐渐增强;
③同周期元素的最高价氧化物对应水化物的碱性从左到右逐渐减弱;
④同主族元素的氢化物的稳定性从上到下逐渐减弱;
⑤同周期元素的单质的氧化性从左到右逐渐增强,离子的还原性逐渐减弱.
(3)元素性质呈周期性变化的决定因素是元素原子核外电子排布呈周期性变化.
解答:解:(1)①根据元素周期表的排布规律:同主族元素的原子最外层电子数相同,均等于族序数,即ⅡA族元素的最外层电子数均为2,故答案为:a;
②根据元素周期律,ⅦA族元素氢化物的沸点从上到下逐渐升高,但是在HF中含有氢键,导致其沸点最高,
故答案为:c;
③O2-、F-、Na+、Mg2+、Al3+电子层排布一样,则核电荷数越多半径越小,即O2-、F-、Na+、Mg2+、Al3+的离子半径逐渐减小,故答案为:b;
④同周期元素的最高化合价从左到右逐渐升高,故答案为:e;
⑤周期元素的原子半径从左到右依次减小,故答案为:b;
(2)①根据元素周期律:同主族元素的单质的氧化性从上到下逐渐减弱,所以氧化性Cl2>Br2,故答案为:>;
②同周期元素的最高价氧化物对应水化物的酸性从左到右逐渐增强,P和S是同一周期元素的原子,
所以酸性:H3PO4<H2SO4,故答案为:<;
③金属镁和铝是同一周期元素原子,同周期元素的最高价氧化物对应水化物的碱性从左到右逐渐减弱,
所以碱性 Mg(OH)2>Al(OH)3,故答案为:>;
④同S和O是同一主族元素的原子,同一主族元素的氢化物的稳定性从上到下逐渐减弱,所以稳定性 H2S<H2O,
故答案为:<;
⑤同周期元素的单质的氧化性从左到右逐渐增强,所以氧化性是S2->Cl-,离子的还原性越弱,则离子的还原性越强,所以还原性H2S>HCl,故答案为:>;
(3)元素性质呈周期性变化的决定因素是元素原子核外电子排布呈周期性变化,故选:C.
②根据元素周期律,ⅦA族元素氢化物的沸点从上到下逐渐升高,但是在HF中含有氢键,导致其沸点最高,
故答案为:c;
③O2-、F-、Na+、Mg2+、Al3+电子层排布一样,则核电荷数越多半径越小,即O2-、F-、Na+、Mg2+、Al3+的离子半径逐渐减小,故答案为:b;
④同周期元素的最高化合价从左到右逐渐升高,故答案为:e;
⑤周期元素的原子半径从左到右依次减小,故答案为:b;
(2)①根据元素周期律:同主族元素的单质的氧化性从上到下逐渐减弱,所以氧化性Cl2>Br2,故答案为:>;
②同周期元素的最高价氧化物对应水化物的酸性从左到右逐渐增强,P和S是同一周期元素的原子,
所以酸性:H3PO4<H2SO4,故答案为:<;
③金属镁和铝是同一周期元素原子,同周期元素的最高价氧化物对应水化物的碱性从左到右逐渐减弱,
所以碱性 Mg(OH)2>Al(OH)3,故答案为:>;
④同S和O是同一主族元素的原子,同一主族元素的氢化物的稳定性从上到下逐渐减弱,所以稳定性 H2S<H2O,
故答案为:<;
⑤同周期元素的单质的氧化性从左到右逐渐增强,所以氧化性是S2->Cl-,离子的还原性越弱,则离子的还原性越强,所以还原性H2S>HCl,故答案为:>;
(3)元素性质呈周期性变化的决定因素是元素原子核外电子排布呈周期性变化,故选:C.
点评:本题考查学生元素周期律的有关知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
科学家一直致力于研究常温、常压下“人工固氮”的新方法.曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3.进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、N2压力1.0×105 Pa、反应时间3h):
相应的化学方程式:N2(g)+3H2O(l)?2NH3(g)+
O2(g)△H=+765.2kJ?mol-1
回答下列问题:
(1)该反应在较低温度下能否自发进行? ;
(2)从323K到353K,氨气的生成量减少的原因 ;
(3)请画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化示意图1,并进行必要标注;
(4)工业合成氨的反应为N2(g)+3H2(g)?2NH3(g).设在容积为2.0L的密闭容器中充入0.60mol N2(g)和1.60mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
.该条件下反应2NH3(g)?N2(g)+3H2(g)的平衡常数为 ;
(5)利用N2和H2可以实验NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ?mol-1
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
则氨气经催化氧化生成一氧化氮气体和水蒸气的热化学方程式为 ;
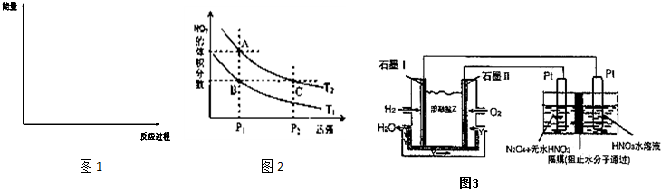
(6)对反应N2O4(g)?2NO2(g),在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示.下列说法正确的是 ;
A.A、C两点的反应速率:A>C
B.B、C两点的气体的平均相对分子质量:B<C
C.A、C两点气体的颜色:A深,C浅
D.由状态B到状态A,可以用加热的方法
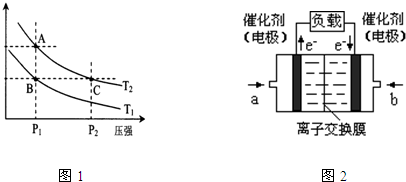
(7)现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备N2O5,装置如图3所示,其中Y为CO2.写出石墨I电极上发生反应的电极反应式 ;在电解池中生成1molN2O5转移电子的物质的量为 .
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 | 2.0 |
| 3 |
| 2 |
回答下列问题:
(1)该反应在较低温度下能否自发进行?
(2)从323K到353K,氨气的生成量减少的原因
(3)请画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化示意图1,并进行必要标注;

(4)工业合成氨的反应为N2(g)+3H2(g)?2NH3(g).设在容积为2.0L的密闭容器中充入0.60mol N2(g)和1.60mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
| 4 |
| 7 |
(5)利用N2和H2可以实验NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ?mol-1
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
则氨气经催化氧化生成一氧化氮气体和水蒸气的热化学方程式为
(6)对反应N2O4(g)?2NO2(g),在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示.下列说法正确的是
A.A、C两点的反应速率:A>C
B.B、C两点的气体的平均相对分子质量:B<C
C.A、C两点气体的颜色:A深,C浅
D.由状态B到状态A,可以用加热的方法
(7)现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备N2O5,装置如图3所示,其中Y为CO2.写出石墨I电极上发生反应的电极反应式
 室温下,将1.00mol/L盐酸滴入20.00mL 1.00mol/L氨水中,溶液pH和温度(℃)
室温下,将1.00mol/L盐酸滴入20.00mL 1.00mol/L氨水中,溶液pH和温度(℃)



