��Ŀ����
��ҵ��һ���ں����ܱ������п��Բ������з�Ӧ�ϳɼ״���CO��g��+2H2��g��?CH3OH��g����H
��1���жϷ�Ӧ�ﵽƽ��״̬��������
a�� ����CH3OH������������CO���������
b�� ���������ܶȲ���
c�� �����������ƽ��������������
d�� CH3OH��CO��H2��Ũ�ȶ����ٷ����仯
��2���±����������Ƿ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
���ɱ��������жϡ�H
��Ҫ���CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ��
a������ b��������� c������CO��Ũ��
d������H2��ѹ e��������������ѹ f��������״�
��ij�¶��£���2mol CO��6mol H2����2L���ܱ������У���ַ�Ӧ10min�ﵽƽ��ʱ���c��CO��=0.2mol/L����CO��ת����Ϊ
��3��ͼ1��ʾ���¶ȷֱ�ΪT1��T2ʱ��ƽ����ϵ��H2�����������ѹǿ�仯���ߣ�A��C����ķ�Ӧ����A
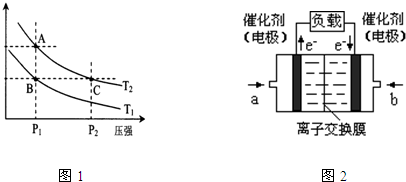
��4��һ�������£�0.5mol�״�������ȫȼ�����ɶ�����̼�����Һ̬ˮ���ų�QKJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ
��1���жϷ�Ӧ�ﵽƽ��״̬��������
cd
cd
������ţ���a�� ����CH3OH������������CO���������
b�� ���������ܶȲ���
c�� �����������ƽ��������������
d�� CH3OH��CO��H2��Ũ�ȶ����ٷ����仯
��2���±����������Ƿ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
��
��
0 �����������=������������Ҫ���CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ��
df
df
������ţ���a������ b��������� c������CO��Ũ��
d������H2��ѹ e��������������ѹ f��������״�
��ij�¶��£���2mol CO��6mol H2����2L���ܱ������У���ַ�Ӧ10min�ﵽƽ��ʱ���c��CO��=0.2mol/L����CO��ת����Ϊ
80%
80%
����ʱ���¶�Ϊ250��
250��
����CH3OH��ʾ�ù��̵ķ�Ӧ����v��CH3OH��=0.08
0.08
mol/��L?min������3��ͼ1��ʾ���¶ȷֱ�ΪT1��T2ʱ��ƽ����ϵ��H2�����������ѹǿ�仯���ߣ�A��C����ķ�Ӧ����A
��
��
C�����������=����������ͬ����A��C����Ļ�ѧƽ�ⳣ��A=
=
C����״̬B��״̬A���ɲ�������
����
�ķ���������¡����¡�����
��4��һ�������£�0.5mol�״�������ȫȼ�����ɶ�����̼�����Һ̬ˮ���ų�QKJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ
2CH3OH��g��+3O2��g��=2CO2��g��+4H2O��l����H=-4QkJ/mol
2CH3OH��g��+3O2��g��=2CO2��g��+4H2O��l����H=-4QkJ/mol
��ͼ2�Ǽ״�ȼ�ϵ�أ��������ҺΪKOH��Һ���ṹʾ��ͼ��д�� a���缫�Ϸ����ĵ缫��ӦʽCH3OH-6e-+8OH-=CO32-+6H2O
CH3OH-6e-+8OH-=CO32-+6H2O
����������1��a��CH3OH������������CO���������ʶ���ʾ����Ӧ���ʣ�
b����Ϊ���壬������������䣬�����������������䣬�ܶ���ʼ����Ϊ��ֵ��
c�������������������䣬�淴Ӧ���У����������ܵ����ʵ�����С����ƽ����Է���������С�����Ϊ��ֵ��
d�����淴Ӧ�õ�ƽ�⣬��Ӧ������Ũ�ȡ�����Ϊ��ֵ��
��2�����ɱ������ݿ�֪���¶�Խ�ߣ�ƽ�ⳣ��ԽС��˵�������¶�ƽ�����淴Ӧ�ƶ��������¶�ƽ�������ȷ�Ӧ�ƶ���
��Ҫ���CO��ת���ʣ�ƽ��Ӧ������Ӧ�ƶ����ݴ˽��ѡ������жϣ�ע����ֻ����COŨ�ȣ�ƽ��������Ӧ�ƶ���CO��ת���ʽ��ͣ�
�ۼ���ƽ��ʱCO�����ʵ�����n��ʼ��CO��-nƽ����CO��=nת����CO��������ת���ʶ������CO��ת���ʣ�
������¶��µ�ƽ�ⳣ�����Աȱ��������ж��¶ȣ�
����v=
����v��CO����������֮�ȵ��ڻ�ѧ������֮�ȼ���v��CH3OH����
��3��ѹǿԽ��Ӧ����Խ�죻ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶Ȳ��䣬ƽ�ⳣ�����䣮ƽ����ϵ��H2����������¶�T1��T2ʱ�ĵͣ�˵��T1��T2��ȣ�ƽ��������Ӧ�ƶ����÷�Ӧ����ӦΪ���ȷ�Ӧ�����¶�T1��T2��
��4��0.5mol�״�������ȫȼ�����ɶ�����̼�����Һ̬ˮ���ų�QKJ���������ݴ˸����Ȼ�ѧ����ʽ��дԭ����д��
��ͼ2�е��������·���ƶ���֪��aΪ������bΪ������ԭ��ظ�������������Ӧ��CH3OH�ڸ����ŵ磬���������ŵ�����̼�����ˮ��
b����Ϊ���壬������������䣬�����������������䣬�ܶ���ʼ����Ϊ��ֵ��
c�������������������䣬�淴Ӧ���У����������ܵ����ʵ�����С����ƽ����Է���������С�����Ϊ��ֵ��
d�����淴Ӧ�õ�ƽ�⣬��Ӧ������Ũ�ȡ�����Ϊ��ֵ��
��2�����ɱ������ݿ�֪���¶�Խ�ߣ�ƽ�ⳣ��ԽС��˵�������¶�ƽ�����淴Ӧ�ƶ��������¶�ƽ�������ȷ�Ӧ�ƶ���
��Ҫ���CO��ת���ʣ�ƽ��Ӧ������Ӧ�ƶ����ݴ˽��ѡ������жϣ�ע����ֻ����COŨ�ȣ�ƽ��������Ӧ�ƶ���CO��ת���ʽ��ͣ�
�ۼ���ƽ��ʱCO�����ʵ�����n��ʼ��CO��-nƽ����CO��=nת����CO��������ת���ʶ������CO��ת���ʣ�
������¶��µ�ƽ�ⳣ�����Աȱ��������ж��¶ȣ�
����v=
| ��c |
| ��t |
��3��ѹǿԽ��Ӧ����Խ�죻ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶Ȳ��䣬ƽ�ⳣ�����䣮ƽ����ϵ��H2����������¶�T1��T2ʱ�ĵͣ�˵��T1��T2��ȣ�ƽ��������Ӧ�ƶ����÷�Ӧ����ӦΪ���ȷ�Ӧ�����¶�T1��T2��
��4��0.5mol�״�������ȫȼ�����ɶ�����̼�����Һ̬ˮ���ų�QKJ���������ݴ˸����Ȼ�ѧ����ʽ��дԭ����д��
��ͼ2�е��������·���ƶ���֪��aΪ������bΪ������ԭ��ظ�������������Ӧ��CH3OH�ڸ����ŵ磬���������ŵ�����̼�����ˮ��
����⣺��1��a��CH3OH������������CO���������ʶ���ʾ����Ӧ���ʣ���ʼ���շ�Ӧ���ʶ���1��1���У�����˵������ƽ�⣬��a����
b����Ϊ���壬������������䣬�����������������䣬�ܶ���ʼ����Ϊ��ֵ������˵�����淴Ӧ����ƽ�⣬��b����
c�������������������䣬�淴Ӧ���У����������ܵ����ʵ�����С����ƽ����Է���������С�����Ϊ��ֵ��˵�����淴Ӧ����ƽ��״̬����c��ȷ��
d��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯��˵�����淴Ӧ����ƽ��״̬����d��ȷ��
��ѡ��cd��
��2�����ɱ������ݿ�֪���¶�Խ�ߣ�ƽ�ⳣ��ԽС��˵�������¶�ƽ�����淴Ӧ�ƶ��������¶�ƽ�������ȷ�Ӧ�ƶ���������ӦΪ���ȷ�Ӧ������H��0��
�ʴ�Ϊ������
��a�������¶ȣ�ƽ�����淴Ӧ�ƶ���ƽ��ʱCO��ת���ʼ�С����a����
b��������������̵���ƽ��ʱ�䣬ƽ�ⲻ�ƶ���COת���ʲ��䣬��b����
c������CO��Ũ�ȣ�ƽ��������Ӧ�ƶ���ƽ��ʱCO��ת���ʼ�С����c����
d������H2��ѹ��ƽ��������Ӧ�ƶ���ƽ��ʱCO��ת��������d��ȷ��
e��������������ѹ����Ӧ������Ũ�Ȳ��䣬�仯���ƶ�����e����
f��������״���ƽ��������Ӧ�ƶ���ƽ��ʱCO��ת��������f��ȷ��
��ѡ��df��
��ij�¶��£���2mol CO��6mol H2����2L���ܱ������У���ַ�Ӧ10min�ﵽƽ��ʱ���c��CO��=0.2mol/L��
ƽ��ʱCO�����ʵ���Ϊ0.2mol/L��2L=0.4mol������CO��ת����Ϊ
��100%=80%��
���ڿ��淴Ӧ��CO��g��+2H2��g��?CH3OH��g��
��ʼ��mol/L����1 3 0
�仯��mol/L����0.8 1.6 0.8
ƽ�⣨mol/L����0.2 1.4 0.8
���Ը��¶���ƽ�ⳣ��k=
=2.041��ƽ�ⳣ��ֻ���¶�Ӱ�죬�ʸ��¶�Ϊ250�森
v��CO��=
=0.08mol/��L?min��������֮�ȵ��ڻ�ѧ������֮�ȣ���v��CH3OH��=v��CO��=0.08mol/��L?min����
�ʴ�Ϊ��80%��250�棻0.08��
��3����ͼ��֪��C��ѹǿ��A��ѹǿ��ѹǿԽ��Ӧ����Խ�죬�ʷ�Ӧ����A��C��
��ͼ��֪A��C�����¶���ͬ��ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶Ȳ���ƽ�ⳣ�����䣬��ƽ�ⳣ��A=C��
��ͼ��֪��ѹǿ��ͬʱ��ƽ����ϵ��H2����������¶�T1��T2ʱ�ĵͣ�˵��T1��T2��ȣ�ƽ��������Ӧ�ƶ����÷�Ӧ����ӦΪ���ȷ�Ӧ�������¶�ƽ������ȷ�Ӧ�ƶ������¶�T1��T2����״̬B��״̬A���ɲ������µķ�����
�ʴ�Ϊ������=�����£�
��4��0.5mol�״�������ȫȼ�����ɶ�����̼�����Һ̬ˮ���ų�QKJ���������Ȼ�ѧ����ʽΪ2CH3OH��g��+3O2��g��=2CO2��g��+4H2O��l����H=-4Q kJ/mol��
��ͼ2�е��������·���ƶ���֪��aΪ������bΪ������ԭ��ظ�������������Ӧ��CH3OH�ڸ����ŵ磬���������ŵ�����̼�����ˮ����ⷴӦʽΪCH3OH-6e-+8OH-=CO32-+6H2O��
�ʴ�Ϊ��2CH3OH��g��+3O2��g��=2CO2��g��+4H2O��l����H=-4Q kJ/mol��CH3OH-6e-+8OH-=CO32-+6H2O��
b����Ϊ���壬������������䣬�����������������䣬�ܶ���ʼ����Ϊ��ֵ������˵�����淴Ӧ����ƽ�⣬��b����
c�������������������䣬�淴Ӧ���У����������ܵ����ʵ�����С����ƽ����Է���������С�����Ϊ��ֵ��˵�����淴Ӧ����ƽ��״̬����c��ȷ��
d��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯��˵�����淴Ӧ����ƽ��״̬����d��ȷ��
��ѡ��cd��
��2�����ɱ������ݿ�֪���¶�Խ�ߣ�ƽ�ⳣ��ԽС��˵�������¶�ƽ�����淴Ӧ�ƶ��������¶�ƽ�������ȷ�Ӧ�ƶ���������ӦΪ���ȷ�Ӧ������H��0��
�ʴ�Ϊ������
��a�������¶ȣ�ƽ�����淴Ӧ�ƶ���ƽ��ʱCO��ת���ʼ�С����a����
b��������������̵���ƽ��ʱ�䣬ƽ�ⲻ�ƶ���COת���ʲ��䣬��b����
c������CO��Ũ�ȣ�ƽ��������Ӧ�ƶ���ƽ��ʱCO��ת���ʼ�С����c����
d������H2��ѹ��ƽ��������Ӧ�ƶ���ƽ��ʱCO��ת��������d��ȷ��
e��������������ѹ����Ӧ������Ũ�Ȳ��䣬�仯���ƶ�����e����
f��������״���ƽ��������Ӧ�ƶ���ƽ��ʱCO��ת��������f��ȷ��
��ѡ��df��
��ij�¶��£���2mol CO��6mol H2����2L���ܱ������У���ַ�Ӧ10min�ﵽƽ��ʱ���c��CO��=0.2mol/L��
ƽ��ʱCO�����ʵ���Ϊ0.2mol/L��2L=0.4mol������CO��ת����Ϊ
| 2mol-0.4mol |
| 2mol |
���ڿ��淴Ӧ��CO��g��+2H2��g��?CH3OH��g��
��ʼ��mol/L����1 3 0
�仯��mol/L����0.8 1.6 0.8
ƽ�⣨mol/L����0.2 1.4 0.8
���Ը��¶���ƽ�ⳣ��k=
| 0.8 |
| 0.2��1.42 |
v��CO��=
| 1mol/L-0.2mol/L |
| 10min |
�ʴ�Ϊ��80%��250�棻0.08��
��3����ͼ��֪��C��ѹǿ��A��ѹǿ��ѹǿԽ��Ӧ����Խ�죬�ʷ�Ӧ����A��C��
��ͼ��֪A��C�����¶���ͬ��ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶Ȳ���ƽ�ⳣ�����䣬��ƽ�ⳣ��A=C��
��ͼ��֪��ѹǿ��ͬʱ��ƽ����ϵ��H2����������¶�T1��T2ʱ�ĵͣ�˵��T1��T2��ȣ�ƽ��������Ӧ�ƶ����÷�Ӧ����ӦΪ���ȷ�Ӧ�������¶�ƽ������ȷ�Ӧ�ƶ������¶�T1��T2����״̬B��״̬A���ɲ������µķ�����
�ʴ�Ϊ������=�����£�
��4��0.5mol�״�������ȫȼ�����ɶ�����̼�����Һ̬ˮ���ų�QKJ���������Ȼ�ѧ����ʽΪ2CH3OH��g��+3O2��g��=2CO2��g��+4H2O��l����H=-4Q kJ/mol��
��ͼ2�е��������·���ƶ���֪��aΪ������bΪ������ԭ��ظ�������������Ӧ��CH3OH�ڸ����ŵ磬���������ŵ�����̼�����ˮ����ⷴӦʽΪCH3OH-6e-+8OH-=CO32-+6H2O��
�ʴ�Ϊ��2CH3OH��g��+3O2��g��=2CO2��g��+4H2O��l����H=-4Q kJ/mol��CH3OH-6e-+8OH-=CO32-+6H2O��
���������⿼��ƽ��״̬�жϡ�ƽ���ƶ���ƽ�ⳣ������Ӧ���ʼ��㡢�Ȼ�ѧ����ʽ��ԭ��ء���ѧƽ��ͼ��ȣ��ǻ�ѧ��Ӧ�����뻯ѧƽ����ۺ���Ŀ���ѶȲ���ע�ػ���֪ʶ�Ŀ��飬��4���е缫��Ӧʽ����дΪ�ѵ㡢�״��㣬������д����Ϊ��������Ӧʽ�������ܷ�Ӧʽ��ȥ������Ӧʽ��Ϊ������Ӧʽ��

��ϰ��ϵ�д�
 �����ߴ���ϵ�д�
�����ߴ���ϵ�д�
�����Ŀ
 CH3OH��g����H
CH3OH��g����H