题目内容
【题目】物质A、B、C、D、E、F、G、H、I、J、K有下图转化关系,其中气体D、E为单质,气体B溶于水显强酸性,试回答:
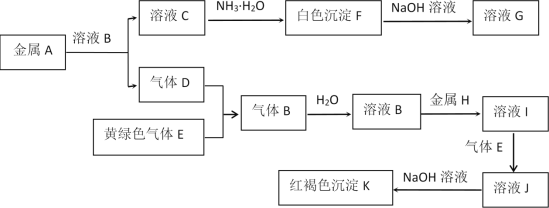
(1)写出下列物质的化学式:A是________,K是__________,
(2)写出反应“C→F”的离子方程式:____________________;
(3)写出反应“F→G”的化学方程式:____________________________;
(4)在溶液I中滴入NaOH溶液,可观察到的现象是:_______。
(5)实验室检验溶液B中阴离子的方法是:________________。
【答案】Al Fe(OH)3 A13+ +3NH3.H2O==Al(OH)3↓十3NH4+ Al(OH)3+NaOH==NaAlO2十2H2O 先生成白色絮状沉淀,而后迅速变为灰绿色,最后变为红褐色沉淀 取少量溶液B于试管中,先滴入少量稀硝酸,再滴加硝酸银溶液
【解析】
K为红褐色沉淀,应为Fe(OH)3,则溶液J中含有Fe3+,气体E是黄绿色气体判断为Cl2,D应为H2, B应为HCl,H为Fe,则I为FeCl2,J为FeCl3,白色沉淀F能溶于过量NaOH溶液,则F为Al(OH)3,G为NaAlO2,A为Al,C为AlCl3;
(1)根据上述分析得A是Al,K是 Fe(OH)3 ,
故答案为:Al;Fe(OH)3;
(2)氯化铝和氨水反应的离子离子方程式为:A13+ +3NH3.H2O=Al(OH)3↓十3NH4+,
故答案为: A13+ +3NH3.H2O=Al(OH)3↓十3NH4+;
(3)氢氧化铝与氢氧化钠反应的化学方程式为:Al(OH)3+NaOH=NaAlO2十2H2O,
故答案为:Al(OH)3+NaOH=NaAlO2十2H2O;
(4)溶液I为氯化亚铁溶液,滴入NaOH溶液,生成氢氧化亚铁,被氧气氧化后生成氢氧化铁,观察到的现象是:先生成白色絮状沉淀,而后迅速变为灰绿色,最后变为红褐色沉淀,
故答案为:先生成白色絮状沉淀,而后迅速变为灰绿色,最后变为红褐色沉淀;
(5)B中阴离子是Cl-,检验方法是:取少量溶液B于试管中,先滴入少量稀硝酸,再滴加硝酸银溶液,
故答案为:取少量溶液B于试管中,先滴入少量稀硝酸,再滴加硝酸银溶液。

