题目内容
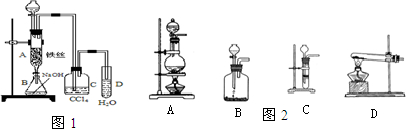
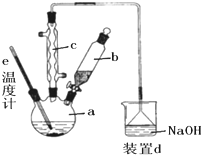
(1)某化学课外小组用右图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.
①据图1写出A中有机反应的化学方程式______
②已知上述有机反应是放热反应.观察到A中的现象是______及______.
③实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是______,写出有关的化学方程式______.
④C中盛放CCl4的作用是______.
⑤能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中滴入AgNO3溶液,若产生淡黄色沉淀,则能证明.另一种验证的方法是向试管D中加入______,现象是______.
(2)图2是乙炔的实验室制法
①反应原理______.
②选择合适的制取实验装置______.
③实验中常用饱和食盐水代替水,目的是______.
④纯净的乙炔气体是无色无味的气体,用电石和水反应制取的乙炔,常含有H2S和PH3而有恶臭气味.可以用______溶液除去杂质气体.
①据图1写出A中有机反应的化学方程式______
②已知上述有机反应是放热反应.观察到A中的现象是______及______.
③实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是______,写出有关的化学方程式______.
④C中盛放CCl4的作用是______.
⑤能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中滴入AgNO3溶液,若产生淡黄色沉淀,则能证明.另一种验证的方法是向试管D中加入______,现象是______.
(2)图2是乙炔的实验室制法
①反应原理______.
②选择合适的制取实验装置______.
③实验中常用饱和食盐水代替水,目的是______.
④纯净的乙炔气体是无色无味的气体,用电石和水反应制取的乙炔,常含有H2S和PH3而有恶臭气味.可以用______溶液除去杂质气体.

(1)①在催化剂的作用下,苯环上的氢原子被溴原子所取代,生成溴苯,同时有溴化氢生成,故答案为:C6H6+Br2
C6H5Br+HBr;
②由于反应放热,苯和液溴均易挥发,溴蒸气是一种红棕色的气体,故答案为:反应液微沸;有红棕色气体充满A容器;
③A中的溴和氢氧化钠反应,可以将溴苯中的溴除去,即Br2+2NaOH=NaBr+NaBrO+H2O或是3Br2+6NaOH=5NaBr+NaBrO3+3H2O,
故答案为:除去溶于溴苯中的溴;Br2+2NaOH=NaBr+NaBrO+H2O或3Br2+6NaOH=5NaBr+NaBrO3+3H2O;
④根据相似相溶原理,溴极易溶于四氯化碳,而溴化氢则不溶,所以C中盛放CCl4的作用是除去溴化氢气体中的溴蒸气,故答案为:除去溴化氢气体中的溴蒸气;
⑤如果发生取代反应,生成溴化氢,溴化氫易溶于水电离出H+和Br-,只要检验含有氢离子或溴离子即可,溴离子的检验:取溶液滴加硝酸银溶液,如果生成淡黄色沉淀就证明是溴离子;氢离子的检验:如果能使紫色石蕊试液变红,就证明含有氢离子,故答案为:石蕊试液;溶液变红色.
(2))①实验室制取乙炔是利用电石和水反应制取的,方程式是CaC2+2H2O→C2H2↑+Ca(OH)2,
故答案为:CaC2+2H2O→C2H2↑+Ca(OH)2;
②由于反应不能加热,所以选项A和D都是错误的,生成气体,不能用长颈漏斗,防止气体逸出,则C错误,可用B制取,故答案为:B;
③由于电石和水的反应很剧烈,所以实验中常用饱和食盐水代替水,目的减缓电石与水的反应速率,故答案为:减缓电石与水的反应速率;
④H2S和PH3都能和硫酸铜溶液反应,因此可以用硫酸铜溶液除去该杂质气体,故答案为:硫酸铜.
| Fe |
②由于反应放热,苯和液溴均易挥发,溴蒸气是一种红棕色的气体,故答案为:反应液微沸;有红棕色气体充满A容器;
③A中的溴和氢氧化钠反应,可以将溴苯中的溴除去,即Br2+2NaOH=NaBr+NaBrO+H2O或是3Br2+6NaOH=5NaBr+NaBrO3+3H2O,
故答案为:除去溶于溴苯中的溴;Br2+2NaOH=NaBr+NaBrO+H2O或3Br2+6NaOH=5NaBr+NaBrO3+3H2O;
④根据相似相溶原理,溴极易溶于四氯化碳,而溴化氢则不溶,所以C中盛放CCl4的作用是除去溴化氢气体中的溴蒸气,故答案为:除去溴化氢气体中的溴蒸气;
⑤如果发生取代反应,生成溴化氢,溴化氫易溶于水电离出H+和Br-,只要检验含有氢离子或溴离子即可,溴离子的检验:取溶液滴加硝酸银溶液,如果生成淡黄色沉淀就证明是溴离子;氢离子的检验:如果能使紫色石蕊试液变红,就证明含有氢离子,故答案为:石蕊试液;溶液变红色.
(2))①实验室制取乙炔是利用电石和水反应制取的,方程式是CaC2+2H2O→C2H2↑+Ca(OH)2,
故答案为:CaC2+2H2O→C2H2↑+Ca(OH)2;
②由于反应不能加热,所以选项A和D都是错误的,生成气体,不能用长颈漏斗,防止气体逸出,则C错误,可用B制取,故答案为:B;
③由于电石和水的反应很剧烈,所以实验中常用饱和食盐水代替水,目的减缓电石与水的反应速率,故答案为:减缓电石与水的反应速率;
④H2S和PH3都能和硫酸铜溶液反应,因此可以用硫酸铜溶液除去该杂质气体,故答案为:硫酸铜.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
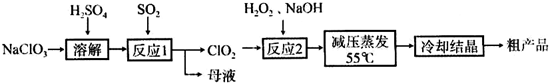
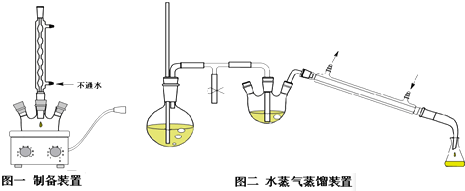
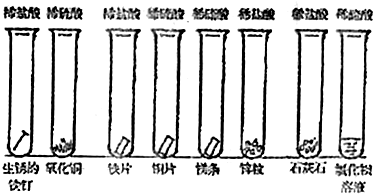
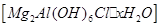 是一种新型离子交换材料,其在高温下完全分解为
是一种新型离子交换材料,其在高温下完全分解为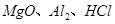 和水蒸气,现用题27图装置进行试验确定其化学式(固定装置略去)。
和水蒸气,现用题27图装置进行试验确定其化学式(固定装置略去)。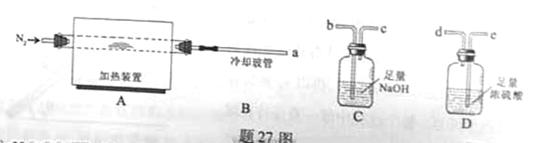
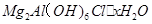 热分解的化学方程式为 。
热分解的化学方程式为 。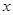 ,则装置的连接顺序为 (按气流方向,用接口字母表示),其中C的作用是 。装置连接后,首先要进行的操作名称是 。
,则装置的连接顺序为 (按气流方向,用接口字母表示),其中C的作用是 。装置连接后,首先要进行的操作名称是 。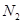 排尽装置中的空气,称取C、D的初始质量后,再持续通入
排尽装置中的空气,称取C、D的初始质量后,再持续通入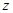 ,除测定D的增重外,至少还需测定 .
,除测定D的增重外,至少还需测定 .