��Ŀ����
����Ŀ����.һ���¶��£���2 L���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯��������ͼ��ʾ��
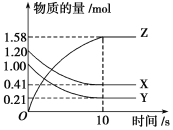
��1���ӷ�Ӧ��ʼ��10 sʱ����Z��ʾ�ķ�Ӧ����Ϊ_____________________________��
��2���÷�Ӧ�Ļ�ѧ����ʽΪ__________________________________________________��
��.�ں��º��ݵ��ܱ������У����������������ٷ����仯ʱ���ٻ�������ѹǿ���ڻ��������ܶȣ��ۻ������������ʵ������ܻ�������ƽ����Է����������ݻ���������ɫ������Ӧ���������ķ�Ӧ����֮�ȵ��ڻ�ѧ������֮��
��1��һ����֤��2SO2(g)��O2(g)![]() 2SO3(g)�ﵽƽ��״̬����_______������ţ���ͬ����
2SO3(g)�ﵽƽ��״̬����_______������ţ���ͬ����
��2��һ����֤��I2(g)��H2(g)![]() 2HI(g)�ﵽƽ��״̬���� ____________��
2HI(g)�ﵽƽ��״̬���� ____________��
��3��һ����֤��A(s)��2B(g)![]() C(g)��D(g)�ﵽƽ��״̬����_________��
C(g)��D(g)�ﵽƽ��״̬����_________��
���𰸡���.��1��0.079 mol��L��1��s��1 ��2��X(g)��Y(g)![]() 2Z(g) ��.��1���٢ۢ� ��2���� ��3���ڢ�
2Z(g) ��.��1���٢ۢ� ��2���� ��3���ڢ�
��������
�����������.��1���ӷ�Ӧ��ʼ��10 sʱ��Z�����ʵ���������1.58mol��Ũ����1.58mol��2L��0.79mol/L������Z��ʾ�ķ�Ӧ����Ϊ0.79mol/L��10s��0.079mol/(L��s)��
��2������ͼ���֪X��Y�����ʵ�����С���Ƿ�Ӧ�ƽ��ʱ�仯���ֱ���1.20mol��0.41mol��0.79mol��1.00mol��0.21mol��0.79mol��Z�����ʵ���������1.58mol��Z����������ݱ仯��֮������Ӧ�Ļ�ѧ������֮�ȿ�֪�÷�Ӧ�Ļ�ѧ����ʽΪX(g)��Y(g)![]() 2Z(g)��
2Z(g)��
�������������ܶ��ǻ������������������ݻ��ı�ֵ����������ƽ����Է��������ǻ��������������ܵ����ʵ����ı�ֵ����ɫ����dz����ɫ�����Ũ���й�ϵ�����κ�ʱ������Ӧ���������ķ�Ӧ����֮�ȵ��ڻ�ѧ������֮������
��1����Ӧ2SO2(g)��O2(g)![]() 2SO3(g)�������С�Ŀ��淴Ӧ����˻�������ѹǿ���������������ʵ�������������ƽ����Է����������������˵���ﵽƽ��״̬��
2SO3(g)�������С�Ŀ��淴Ӧ����˻�������ѹǿ���������������ʵ�������������ƽ����Է����������������˵���ﵽƽ��״̬��
��2����ӦI2(g)��H2(g)![]() 2HI(g)���������Ŀ��淴Ӧ�����ڵ�����ɫ���壬������������ɫ����˵���ﵽƽ��״̬��
2HI(g)���������Ŀ��淴Ӧ�����ڵ�����ɫ���壬������������ɫ����˵���ﵽƽ��״̬��
��3����ӦA(s)��2B(g)![]() C(g)��D(g)���������ģ���������������ӵĿ��淴Ӧ��������������ܶ�����������ƽ����Է���������������˵���ﵽƽ��״̬��
C(g)��D(g)���������ģ���������������ӵĿ��淴Ӧ��������������ܶ�����������ƽ����Է���������������˵���ﵽƽ��״̬��