题目内容
【题目】如图制取SO2并验证SO2性质的装置图。
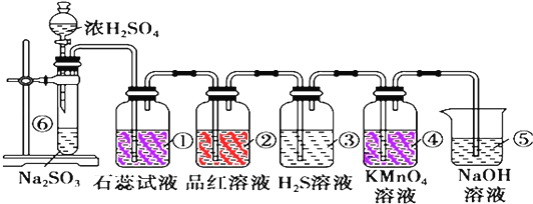
已知Na2SO3+H2SO4=Na2SO4+SO2+H2O。
(1)①中为紫色石蕊试液,实验现象为________,实验证明SO2是________气体。
(2)②中为红色品红溶液,现象为________证,明SO2有________性。
(3)④为紫红色高锰酸钾,实验现象为________,证明SO2有________性。
(4)⑤的作用________,反应方程式_________________________________。
【答案】溶液变红 酸性 褪色 漂白性 紫红色褪去 还原性 吸收多余SO2,防止污染环境 SO2+2NaOH=Na2SO3+H2O
【解析】
二氧化硫是一种酸性氧化物,具有酸性氧化物的通性,二氧化硫中S元素是+4价,处于中间价态,既有氧化性还有还原性,另外二氧化硫还具有漂白,据此解答。
(1)二氧化硫为酸性氧化物与水反应生成亚硫酸,亚硫酸电离产生氢离子,溶液显酸性,遇石蕊显红色,即①中实验现象为溶液变红,实验证明SO2是酸性气体;
(2)二氧化硫与品红化合生成无色物质,能使品红溶液褪色,故二氧化硫具有漂白性,即②中现象为褪色;
(3)酸性KMnO4具有强氧化性,溶液颜色为紫红色,SO2中+4价S具有还原性,二氧化硫通入酸性高锰酸钾中发生反应:2KMnO4+5SO2+2H2O=K2SO4+2MnSO4+2H2SO4,该反应中二氧化硫为还原剂,具有还原性,发生氧化反应,导致酸性KMnO4溶液的紫红色褪去;
(4)二氧化硫有毒,不能直接排放到空气中,二氧化硫是酸性氧化物能够与氢氧化钠反应生成亚硫酸钠和水,所以可以用氢氧化钠溶液吸收二氧化硫,防止污染环境,反应的化学方程式为:2NaOH+SO2=Na2SO3+H2O。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案【题目】25℃时,有关物质的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)请写出H2SO3的电离平衡常数K1的表达式:________________。
(2) 常温下,将体积为10mL pH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者_____后者(填“>”、“<”或“=”)。
(3)一定条件下,冰醋酸加水稀释过程中溶液导电能力I随加水体积V变化曲线如右图所示,则a、b、c三点溶液醋酸的电离程度由大到小为____________________。

(4)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的关系为___________。
(5)体积相同、c(H+)相同的①CH3COOH;②HCl;③H2SO4 三种酸溶液分别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是_____(填序号)。
(6)已知,H+(aq) + OH-(aq) == H2O(l) ΔH =-57.3 kJ/mol。实验测得稀醋酸与稀NaOH溶液反应生成1 mol H2O时放出57 kJ的热,则醋酸溶液中,醋酸电离的热化学方程式为________________。
【题目】己知下表为25℃时某些弱酸的电离平衡常数。依据所给信息判断,下列说法正确的是
CH3COOH | HClO | H2CO3 |
Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
A. 向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O=2HClO+CO32-
B. 相同浓度的CH3COONa和NaClO的混合溶液中,c(CH3COOH)+c(HClO)=c(OH-)-c(H+)
C. 25℃时,0.10mol·L-1Na2CO3溶液通入CO2至溶液的pH=7时,溶液中:c(Na+)=c(CO32-)+ c (HCO3-)+c(H2CO3)
D. 向0.1mol·L-1CH3COONa溶液中加入少量水,溶液中![]() 增大
增大