题目内容
13.下列操作中所发生的化学反应属于吸热反应的是( )| A. | 氢氧化钡晶体与氯化铵混合研磨 | B. | 用铜与浓硝酸制取NO2 | ||
| C. | 烧碱溶液与硫酸氢钠溶液混合 | D. | 镍镉充电电池放电 |
分析 常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱),以此解答该题.
解答 解:A.氢氧化钡晶体与氯化铵晶体混合,为吸热反应,故A选;
B.铜与浓硝酸制取NO2为放热反应,故B不选;
C.烧碱溶液与硫酸氢钠溶液混合,发生中和反应,为放热反应,故C不选;
D.镍镉充电电池放电,电能转化为化学能,为释放能量的过程,为放热反应,故D不选.
故选A.
点评 本题考查化学反应的热量变化,为高频考点,学生应注重归纳中学化学中常见的吸热或放热的反应,对于特殊过程中的热量变化的要熟练记忆来解答此类习题.

练习册系列答案
相关题目
4.下列物质中,含有共价键的离子化合物是( )
| A. | CaCl2 | B. | Na2O | C. | H2O | D. | NH4Cl |
1.自来水管与下列材料做成的水龙头连接,锈蚀最快的铁水管连接的是( )
| A. | 铜水龙头 | B. | 铁水龙头 | C. | 塑料水龙头 | D. | 陶瓷水龙头 |
8.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 能使pH试纸变深红色的溶液中:Na+、NH4+、I-、NO3- | |
| B. | c(H+)/c(OH-)=1×10 -12的溶液中:K+、Na+、CO32-、SO42- | |
| C. | pH=7的溶液中:K+、NH4+、Fe3+、NO3- | |
| D. | 加入铝粉生成H2的溶液:K+、Mg2+、SO42-、HCO3- |
2.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,11.2 L水中含有的氢原子数为NA | |
| B. | 1 mol•L-1FeCl3溶液中,阳离子数为NA | |
| C. | 一定条件下,将1mol SO2和0.5 mol O2充入一密闭容器内,充分反应后的生成物分子数为NA | |
| D. | 在反应2Na2O2+2CO2═2Na2CO3+O2中,每生成0.5 molO2转移的电子数为NA |
9.某同学用稀NaOH溶液作SO2的尾气吸收液,实验完毕测得吸收液的pH约为10(已知:相同温度下饱和Na2SO3溶液的pH约为9.5),则下列说法正确的是( )
| A. | 该溶液中:c(OH-)>c(Na+)>c(SO32-)>c(HSO3-)>c(H+) | |
| B. | 该溶液中:c(Na+)+c(H+)═c(OH-)+2c(SO32-) | |
| C. | 该溶液的溶质为Na2SO3和NaHSO3 | |
| D. | 该溶液pH约为10的原因是NaOH过量 |
7.化学与生产、生活密切相关,下列有关说法正确的是( )
| A. | 油脂在人体内水解为氨基酸和甘油等小分子物质后才能被吸收 | |
| B. | 用食醋可除去热水壶内壁的水垢 | |
| C. | 石油分馏的目的是获得乙烯、丙烯和丁二烯 | |
| D. | 淀粉和纤维素的分子式为(C6H10O5)n,它们互为同分异构体 |
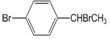 .写出该两步反应所需的试剂及条件:液溴、溴化铁作催化剂,溴、光照
.写出该两步反应所需的试剂及条件:液溴、溴化铁作催化剂,溴、光照 .
.