题目内容
已知0.1mol/L H2SO4在水中的第一步电离是完全的,第二步电离并不完全。常温下有0.1mol/L的以下几种溶液的电离度(即已经电离的分子数占原来分子总数的百分数)如下表,回答下列问题:
| ①H2SO4溶液中的HSO4– | ②NaHSO4溶液中的HSO4– | ③CH3COOH | ④HCl溶液 |
| 10% | 29% | 1.33% | 100% |
(2)常温下,题设条件下的①溶液中c(H+)= 。
(3)常温下,pH相同的上述几种溶液,其物质的量浓度由大到小的顺序是(填序号) 。
(4)若将10mL题设条件下的NaHSO4溶液与0.1mol/LNaOH溶液等体积混合,则混合后溶液中离子浓度由大到小顺序为 。
(5)根据题设条件计算CH3COOH的电离常数Ka= 。若常温下,将b mol·L–1的CH3COONa液与0.01 mol·L–1的盐酸等体积混合,反应达平衡时,测得溶液的pH=7,用含b的代数式表示CH3COOH的电离常数Ka= 。
(1)H2SO4=HSO4–+H+ HSO4– H++ SO42– (2分) (2)0.11 mol·L–1(2分)
H++ SO42– (2分) (2)0.11 mol·L–1(2分)
(3)③②④①或③>②>④>① (2分)
(4)c(Na+)>c(SO42–)>c(OH–)>c(HSO4–)>c(H+) (2分)
(5)1.77×10–5或1.8×10–5 (2分)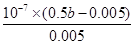 或(b-0.01)×10-5(2分)
或(b-0.01)×10-5(2分)
解析试题分析:(1)已知0.1mol/L H2SO4在水中的第一步电离是完全的,第二步电离并不完全,所以硫酸在水中的电离方程式为H2SO4=HSO4–+H+ HSO4– H++ SO42–。
H++ SO42–。
(2)H2SO4 = HSO4– + H+
0.1mol/L 0.1mol/L 0.1mol/L
HSO4–  H++ SO42–
H++ SO42–
0.1mol/L×10% 0.1mol/L×10%
所以溶液中氢离子浓度=0.1mol/L+0.1mol/L×10%=0.11mol/L
(3)硫酸是二元酸,第一步完全电离,第二步部分电离。盐酸是一元酸,完全电离。硫酸氢钠中HSO4-的电离程度强于醋酸的电离程度,所以常温下,pH相同的上述几种溶液,其物质的量浓度由大到小的顺序是③>②>④>①。
(4)将10mL题设条件下的NaHSO4溶液与0.1mol/LNaOH溶液等体积混合,二者恰好反应生成硫酸钠,但由于SO42-水解SO42-+H2O HSO4-+OH-,因此溶液显碱性。又因为水还电离出OH-,所以溶液中离子浓度大小顺序是c(Na+)>c(SO42–)>c(OH–)>c(HSO4–)>c(H+)。
HSO4-+OH-,因此溶液显碱性。又因为水还电离出OH-,所以溶液中离子浓度大小顺序是c(Na+)>c(SO42–)>c(OH–)>c(HSO4–)>c(H+)。
(5)醋酸的电离度是1.33%,则
CH3COOH CH3COO- + H+
CH3COO- + H+
起始浓度(mol/L) 0.1 0 0
转化浓度(mol/L) 0.1×1.33% 0.1×1.33% 0.1×1.33%
平衡浓度(mol/L)0.1-0.00133 0.00133 0.00133
所以该温度下醋酸的电离常数= =
=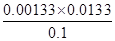 =1.77×10–5
=1.77×10–5
反应达平衡时,测得溶液的pH=7,则根据电荷守恒可知c(CH3COO-)+c(Cl-)+c(OH–)=c(Na+)+c(H+),因此c(OH–)=c(H+)=10-7mol/L、c(CH3COO-)+c(Cl-)=c(Na+)=0.5bmol/L,所以c(CH3COO-)=c(Na+)-c(Cl-)=0.5bmol/L-0.005mol/L。根据物料守恒可知溶液醋酸的浓度是0.5bmol/L-(0.5bmol/L-0.005mol/L)=0.005mol/L,所以该温度下醋酸的电离常数= =
=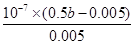 =(b-0.01)×10-5
=(b-0.01)×10-5
考点:考查弱电解质的电离、氢离子浓度与电离平衡常数计算以及溶液中离子浓度大小比较

 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
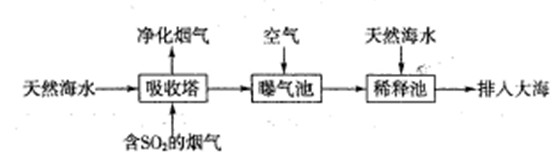
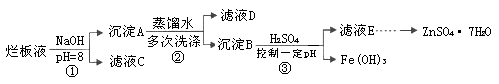
目标测试系列答案利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO。制备流程图如下: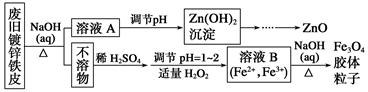
已知:Zn及其化合物的性质与Al及其化合物的性质相似,请回答下列问题:
(1)用NaOH溶液处理废旧镀锌铁皮的作用有________。
| A.去除油污 | B.溶解镀锌层 | C.去除铁锈 | D.钝化 |
(3)由溶液B制取Fe3O4胶体粒子的过程中,须持续通入N2,其原因是
_______________________________________________________________
(4)Fe3O4胶体粒子能否用减压过滤法实现固液分离?__________(填“能”或“不能”),理由是________________________________。
(5)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。若需配制浓度为0.010 00 mol·L-1的K2Cr2O7标准溶液250 mL,应准确称取________ g K2Cr2O7(保留4位有效数字,已知MK2Cr2O7=294.0 g·mol-1)。配制该标准溶液时,下列仪器中不必要用到的有________(用编号表示)。
①电子天平 ②烧杯 ③量筒 ④玻璃棒
⑤容量瓶 ⑥胶头滴管 ⑦移液管
(6) 滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将________(填“偏大”、“偏小”或“不变”)。
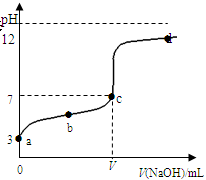
在常温下向20mL 0.1 mol·L-1某酸(用HAc表示)溶液中逐滴加入0.1 mol·L-1 NaOH溶液,用pH计来测定溶液中pH数据如下表,作出pH与NaOH溶液体积关系的曲线如图所示(忽略温度变化)。请根据表中数据和滴定曲线回答以下问题:
| V(NaOH)mL | 0.00 | 10.00 | 18.00 | 19.80 | 19.98 | 20.00 | 20.02 | 20.20 | 22.00 | 40.00 |
| pH | 3.0 | 4.7 | 5.7 | 6.7 | 7.7 | 8.7 | 9.7 | 10.7 | 11.7 | 12.5 |
(2)当V (NaOH)=20.00mL时,请写出溶液中主要存在的两种平衡状态的表示式_______________、________________;溶液中离子浓度由大到小的顺序是___________________;
(3)a、b、c、d四点对应溶液中水的电离程度由大到小的顺序是_________________。
(4)该温度下,滴定曲线上c点时HAc的电离平衡常数Ka=_______(用含V的代数简式表示)。
某学生用0.10 mol/L标准NaOH溶液滴定某浓度的盐酸。记录数据如下:
| 实验序号 | 待测液体积(mL) | 所消耗NaOH标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.54 |
| 2 | 20.00 | 6.00 | 26.00 |
| 3 | 20.00 | 1.40 | 21.36 |
(1)滴定时选用酚酞试液作指示剂,如何判断滴定达到终点 。
(2)盐酸的物质的量浓度为_____________
(3)碱式滴定管尖嘴部分有气泡,滴定后消失,对测定结果的影响是 (填“偏高”或“偏低”或“无影响”,下同)。
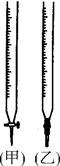
(4)某同学用已知准确浓度的高锰酸钾溶液滴定溶液中Fe2+的浓度,高锰酸钾溶液应盛放在 中(填“甲”或“乙”),该反应的离子方程式为: 。
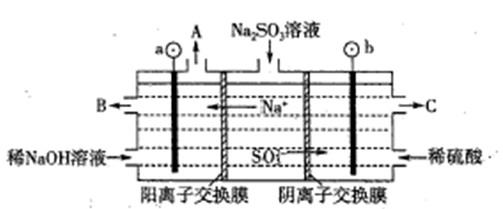
硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为:H2SO4=H++HSO4-,HSO4- H++SO42-.
H++SO42-.
请据此回答下列有关问题:
(1)Na2SO4溶液呈 (填“弱酸性”、“中性”或“弱碱性”),原因是: (用离子方程式表示)
(2)写出H2SO4溶液与BaCl2溶液反应的离子方程式: ;
(3)在0.1 mol·L-1的Na2SO4溶液中,下列粒子浓度关系式正确的是 。(填编号)
| A.c(SO42-)+c(HSO4-)=0.1 mol·L-1 | B.c(SO42-)+c(HSO4-)=2 c(Na+) |
| C.c(OH-)=c(H+)+c(HSO4-) | D.c(Na+)+c(H+)=c(OH-)+c(HSO4-) |
 Fe3+(aq)+3OH-(aq) ; ΔH=" a" kJ?mol-1
Fe3+(aq)+3OH-(aq) ; ΔH=" a" kJ?mol-1