题目内容
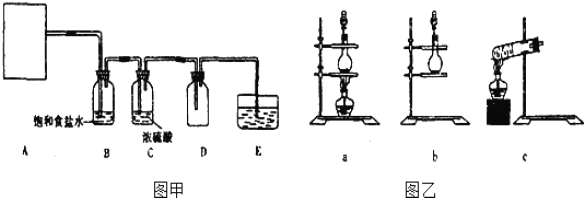
【题目】某学生欲完成反应2Ag+2HCl = 2AgCl↓+H2↑,设计了四个实验,你认为可行的是

A. A B. B C. C D. D
【答案】C
【解析】试题分析:该反应不能自发进行,要使该反应发生,则只能设计成电解池,Ag失电子化合价升高,应该作阳极,其它金属或导电的非金属作阴极,A.要实现该反应2HCl+2Ag═2AgCl↓+H2↑,该装置中应该Ag作阳极、C作阴极,A错误;B.该装置是原电池不是电解池,且发生反应Fe+2HCl=FeCl2+H2↑,B错误;C.该装置是电解池,且Ag作阳极、Ag作阴极,能完成反应2HCl+2Ag═2AgCl↓+H2↑,C正确;D.该装置既不是原电池也不是电解池,Ag和HCl不反应,所以不能完成反应2HCl+2Ag═2AgCl↓+H2↑,D错误,答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目