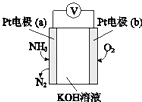
��Ŀ����
����Ŀ������˵����ȷ���ǣ� ��
A.ij�л���ȼ��ֻ����CO2��H2O���Ҷ������ʵ�����ȣ�����л�������ΪCnH2n
B.һ������������������ȼ�ղ�ͨ��ŨH2SO4 �� ���ٵ�����������ɵ�ˮ���������
C.ij��̬��CxHy������O2ǡ����ȫ��Ӧ�������Ӧǰ������������䣨�¶ȣ�100�棩����y=4����������٣���y��4������y��4
D.��ͬ������������ȫȼ�գ�����O2Խ�࣬���к�H%Խ��
���𰸡�D
���������⣺A���������к���̼����Ԫ�أ����������غ㶨�ɿ�֪��������һ������̼����Ԫ�أ���Ԫ�ز���ȷ������ȷ���л������ɣ���A����B��Ũ�������յ���ˮ��������ȼ��ǰ����������Ҳ���ܷ����仯����������������������ȼ�ղ�ͨ��ŨH2SO4 �� ���ٵ������һ��ʱ���ɵ�ˮ�������������B����
C���¶ȣ�100�棬���ɵ�ˮΪ��̬������CxHy+��x+ ![]() ��O2
��O2 ![]() xCO2+
xCO2+ ![]() H2O��g���������Ӧǰ����������������У�1+��x+
H2O��g���������Ӧǰ����������������У�1+��x+ ![]() ��=x+
��=x+ ![]() ����ã�y=4����������٣�1+��x+
����ã�y=4����������٣�1+��x+ ![]() ����x+
����x+ ![]() ����ã�y��4������y��4����C����
����ã�y��4������y��4����C����
D����C��O2��CO2 �� 4H��O2��2H2O���бȽϣ�����1molO2 �� ��Ҫ12gC��������1molO2 �� ��Ҫ4gH����֪�л��ﺬ����Խ������ʱ���ĵ�O2Խ�࣬��D��ȷ��
��ѡ��D��

 ��������ϵ�д�
��������ϵ�д�����Ŀ��������ˮ������ҵ��ɰ�ǡ���֬��Ư����ɱ�������У��������ƣ�NaClO2����������Ҫ�����ã���ͼ�������������ƵĹ�������ͼ�� 
��֪����NaClO2���ܽ�����¶����߶������ʵ������¿ɽᾧ����NaClO23H2O��
�ڳ����£�Ksp��FeS��=6.3��10��18��Ksp��CuS��=6.3��10��36��Ksp��PbS��=8��10��28
�ۢ�װ���е����������Һ����������������ͬʱ�������ᣬ��������������ͬʱ�����������ƣ�
��1��I�з�����Ӧ�����ӷ���ʽΪ ��
��2������Һ�еõ�NaClO23H2O����������������������д��ţ���
a������ b������Ũ�� c������ d����ȴ�ᾧ e������
��3��ӡȾ��ҵ�����������ƣ�NaClO2��Ư��֯�Ư��֯��ʱ���������õ���HClO2 �� ����25��ʱHClO2�����ֳ�������ĵ���ƽ�ⳣ����
���� | HClO2 | HF | H2CO3 | H2S |
Ka/molL��1 | 1��10��2 | 6.3��10��4 | K1=4.30��10��7 | K1=9.1��10��8 |
�ٳ����£����ʵ���Ũ����ȵ�NaClO2��NaF��NaHCO3��Na2S������Һ��pH�ɴ�С��˳��Ϊ���û�ѧʽ��ʾ����
��Na2S�dz��õij�������ij��ҵ��ˮ�к��е�Ũ�ȵ�Cu2+��Fe2+��Pb2+���ӣ��μ�Na2S��Һ�����������ij������������£������һ�����ӳ�����ȫʱ��������Ũ��Ϊ10��5molL��1����ʱ��ϵ�е�S2����Ũ��Ϊ ��
��4����װ��������������a�����Ϊ1.12L����״��������ת�Ƶ��ӵ����ʵ���Ϊ