题目内容
6.宇航员翟志刚成功完成的中国历史上首次太空行走,使中国成为第三个独立掌握出舱活动技术的国家.宇航员出舱时,呼吸所需的氧气主要来自太空服中的呼吸面具.下列物质在一定条件下均能产生氧气,其中最适宜用于呼吸面具中供氧剂的是( )| A. | KMnO4 | B. | H2O2 | C. | KClO3 | D. | Na2O2 |
分析 根据物质与人类呼吸产生的二氧化碳反应能否生成氧气及物质为固体时容易携带等优点来分析.
解答 解:A、KMnO4加热才能分解生成氧气,不适合在太空中使用,故A不选;
B、过氧化氢能分解生成氧气,一般需要催化剂来加快反应速率,且过氧化氢为液体,不方便携带,故B不选;
C、氯酸钾能分解生成氧气,但需要加热、需要催化剂,不适合在太空中使用,故C不选;
D、因过氧化钠为固体,携带方便,且能与人呼吸产生的二氧化碳反应生成氧气,不需要催化剂、不需要加热,则最适宜用于呼吸面具中供氧剂,故D选;
故选D.
点评 本题考查物质的性质,明确物质在什么条件下能反应生成氧气是解答本题的关键,并注意利用物质的状态来解答.

练习册系列答案
相关题目
5.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.1mol Cl2与足量Na0H溶液反应,转移电子的数目为0.2NA | |
| B. | 0.1mol苯乙烯中含有碳碳双键的数目为0.4NA | |
| C. | 4.6g由NO2和N204组成的混合物中含有氧原子的数目为0.2NA | |
| D. | 标准状况下,11.2L乙醇中含有羟基的数目为0.5NA |
17.化学学科中的平衡理论包括:化学平衡、电离平衡、溶解平衡等,且均符合勒夏特列原理.请回答下列问题:
I、在2L密闭容器内,800℃时反应:2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=$\frac{{c}^{2}(N{O}_{2})}{{c}^{2}(NO)×c({O}_{2})}$.已知:K300℃>K350℃,则该反应是放热反应.
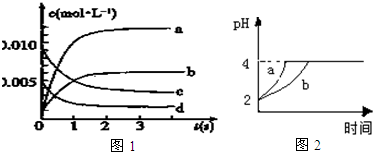
(2)如图1中表示NO2的变化的曲线是b.用O2表示从0~2s内该反应的平均速率v(O2)=1.5×10-3mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是BE.
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.NO、O2、NO2的浓度之比为2:1:2 D.容器内密度保持不变
E.容器内气体的颜色不再变化
(4)缩小容器体积使压强增大,平衡向正反应方向移动(填“正”或“逆”),K值不变(填“增大”、“减小”或“不变”)
II、一定温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g)?2C(g)△H>0,起始时,c(A)=0.2mol/L,c(B)=0.6mol/L,c(C)=0.4mol/L.当平衡时,下列数据可能存在的是bc.
a.c(A)=0.4mol/L b.c(B)=1.0mol/L
c.c(A)=0.3mol/L且c(C)=0.2mol/L d.c(C)=1.0mol/L
III、常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图2所示,则图中表示醋酸溶液中pH变化曲线的是b(填“a”或“b”).设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2,则m1<m2(选填“<”、“=”、“>”).
I、在2L密闭容器内,800℃时反应:2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图1中表示NO2的变化的曲线是b.用O2表示从0~2s内该反应的平均速率v(O2)=1.5×10-3mol•L-1•s-1.

(3)能说明该反应已达到平衡状态的是BE.
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.NO、O2、NO2的浓度之比为2:1:2 D.容器内密度保持不变
E.容器内气体的颜色不再变化
(4)缩小容器体积使压强增大,平衡向正反应方向移动(填“正”或“逆”),K值不变(填“增大”、“减小”或“不变”)
II、一定温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g)?2C(g)△H>0,起始时,c(A)=0.2mol/L,c(B)=0.6mol/L,c(C)=0.4mol/L.当平衡时,下列数据可能存在的是bc.
a.c(A)=0.4mol/L b.c(B)=1.0mol/L
c.c(A)=0.3mol/L且c(C)=0.2mol/L d.c(C)=1.0mol/L
III、常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图2所示,则图中表示醋酸溶液中pH变化曲线的是b(填“a”或“b”).设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2,则m1<m2(选填“<”、“=”、“>”).
1.铁及其化合物在日常生活、生产中应用广泛.
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,工业上利用NaClO 和NaOH的混合溶液将2Fe(OH)3氧化性制备高铁酸钠,反应的化学方程式为2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O;高铁酸钠能用作新型净水剂的原理是本身具有强氧化性可杀菌消毒,在反应中被还原成三价铁离子水解生成氢氧化铁胶体净水;
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆.以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下: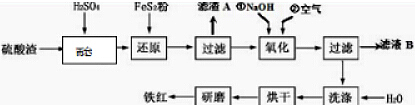
①酸溶过程中发生反应的化学方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O,
Al2O3+3H2SO4═Al2(SO4)3+3H2O,MgO+H2SO4═MgSO4+H2O;“滤渣A”主要成份的化学式为SiO2.
②还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,请写出该反应的离子方程式FeS2+14Fe3++8H2O═15Fe2++2SO42-+16H+;
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为4Fe2++O2+2H2O+8OH-=4Fe(OH)3↓.
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是3.2~3.8,
如果pH过大,可能引起的后果是Al3+、Mg2+形成沉淀,使制得的铁红不纯.
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,工业上利用NaClO 和NaOH的混合溶液将2Fe(OH)3氧化性制备高铁酸钠,反应的化学方程式为2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O;高铁酸钠能用作新型净水剂的原理是本身具有强氧化性可杀菌消毒,在反应中被还原成三价铁离子水解生成氢氧化铁胶体净水;
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆.以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:

①酸溶过程中发生反应的化学方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O,
Al2O3+3H2SO4═Al2(SO4)3+3H2O,MgO+H2SO4═MgSO4+H2O;“滤渣A”主要成份的化学式为SiO2.
②还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,请写出该反应的离子方程式FeS2+14Fe3++8H2O═15Fe2++2SO42-+16H+;
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为4Fe2++O2+2H2O+8OH-=4Fe(OH)3↓.
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是3.2~3.8,
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
11.在pH=1的无色透明溶液中,能够大量共存的离子组是( )
| A. | K+、CO32-、Cl-、NO3- | B. | MnO4-、K+、OH-、SO42- | ||
| C. | Cl-、SO42-、Cu2+、Ba2+ | D. | Mg2+、Na+、NO3-、Cl- |
18.配制NH4Cl溶液时,为了使NH4+浓度与Cl-的浓度比达到1:1,可加入( )
| A. | 适量的HCl | B. | 适量的NaCl | C. | 适量的氨水 | D. | 适量的NaOH |
16.下列实验操作正确的是( )
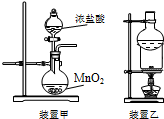

| A. | 用装置甲可以制备氯气 | |
| B. | 用装置乙分离泥沙中的碘单质 | |
| C. | 向碘酒中加入CCl4,静置后分液,可以分离碘酒中的碘 | |
| D. | 用玻璃棒蘸取NaClO溶液点在pH试纸上,测定溶液的pH |