题目内容
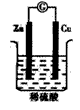
下列关于铜锌原电池(稀硫酸作电解质溶液)的叙述错误的是
A.电子由正极通过导线流向负极 B.负极反应式为:Zn-2e-=Zn2+
C.正极产生1molH2电池转移2mol电子 D.可以用碳棒代替铜片作为正极
【答案】
A
【解析】
试题分析:关于铜锌原电池(稀硫酸作电解质溶液),锌做负极,失去电子,发生氧化反应,Zn-2e-=Zn2+
铜做正极,得到电子,发生还原反应,电子从负极流向正极,电流由正极流向负极,可知A项说法错误。B、C、D说法正确。
考点:铜锌原电池
点评:考查铜锌原电池的构造原理,原电池是历年高考的重点,考生要掌握原电池的形成原理,准确判断。

练习册系列答案
相关题目
下列关于铜锌原电池(稀硫酸作电解质溶液)的叙述错误的是
| A.电子由正极通过导线流向负极 | B.负极反应式为:Zn-2e-=Zn2+ |
| C.正极产生1molH2电池转移2mol电子 | D.可以用碳棒代替铜片作为正极 |
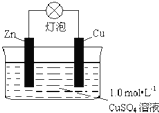 下列关于铜锌原电池(如图)的叙述错误的是( )
下列关于铜锌原电池(如图)的叙述错误的是( )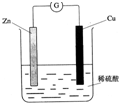 下列关于铜锌原电池(如图所示)的说法正确的是( )
下列关于铜锌原电池(如图所示)的说法正确的是( )