题目内容
【题目】某同学设计如下三个实验方案,以探究某反应是放热反应还是吸热反应:
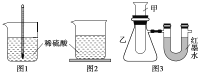
方案一:如图1,在小烧杯里放一些除去氧化铝保护膜的铝片,然后向烧杯里加入10 mL 2 mol/L稀硫酸,再插入一支温度计,温度计的温度由20 ℃逐渐升至75 ℃,随后,温度逐渐下降,最终停留在20 ℃。
方案二:如图2,在烧杯底部用熔融的蜡烛粘一块小木片,在烧杯里加入10 mL 2 mol/L硫酸溶液,再向其中加入氢氧化钠溶液,片刻后提起烧杯,发现小木片脱落下来。
方案三:如图3,甲试管中发生某化学反应,实验前U形管红墨水液面相平,在化学反应过程中,通过U形管两侧红墨水液面高低判断某反应是吸热反应还是放热反应。
序号 | 甲试管里发生反应的物质 | U形管里红墨水液面 |
① | 氧化钙与水 | 左低右高 |
② | 氢氧化钡晶体与氯化铵晶体(充分搅拌) | ? |
③ | 铝片与烧碱溶液 | 左低右高 |
④ | 铜与浓硝酸 | 左低右高 |
根据上述实验回答相关问题:
(1)该铝片与稀硫酸的反应是________(填“吸热”或“放热”)反应。
(2)方案二中,小木片脱落的原因是_________,由此得出的结论是________。
(3)由方案三的现象得出结论:①③④组物质发生的反应都是________(填“吸热”或“放热”)反应。
(4)方案三实验②的U形管中的现象为___________,说明反应物的总能量小于生成物的总能量。
【答案】放热 蜡烛熔化了 氢氧化钠与硫酸的反应放热 放热 红墨水液面左高右低
【解析】
(1)根据温度计由20℃逐渐升至75℃判断;
(2)小木片脱落,说明蜡烛熔化了;
(3)根据液面左低右高的现象,结合热胀冷缩的原理分析判断;
(4)根据反应物总能量小于生成物总能量分析判断。
(1)温度计的温度由20℃逐渐升至75℃,说明铝片与盐酸反应为放热反应,故答案为:放热;
(2)方案二中,氢氧化钠与硫酸的反应放热,温度升高,蜡烛熔化了,因此小木片脱落,故答案为:蜡烛熔化了;氢氧化钠与硫酸的反应放热;
(3)由方案三的现象得出结论:①③④组中出现了液面左低右高的现象,说明锥形瓶中气体的压强增大,根据热胀冷缩,因此发生的反应都是放热反应,故答案为:放热;
(4)氢氧化钡晶体与氯化铵晶体(充分搅拌)反应为典型的吸热反应,故红墨水液面左高右低,反应物总能量低于生成物总能量,故答案为:红墨水液面左高右低。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案