题目内容
8.金属X相对原子质量是金属Y相对原子质量的2/3,等质量的X和Y元素在相同条件下跟过量的盐酸反应,所产生H2的体积前者为后者的一半,则X与Y两元素的化合价为( )| A. | +1,+3 | B. | +3,+1 | C. | +2,+3 | D. | +3,+2 |
分析 在金属和酸的反应中,金属的化合价升高,失电子,氢元素的化合价降低,得电子,在反应中,得失电子守恒,据此设未知数进行计算即可.
解答 解:设金属X的相对原子质量为2a,则Y的相对原子质量为3a;设X的化合价为x,Y的化合价为y,质量均为1g,产生氢气的体积比为1:2,则氢气的物质的量比也为1:2,金属X和酸的反应中电子守恒得到:①$\frac{1}{2a}$(x-0)=2(1-0),金属Y和酸的反应中电子守恒得到:②$\frac{1}{3a}$(y-0)=2×2(1-0),
解得x:y=1:3,即x为+1价,y为+3价.
故选A.
点评 此题考查学生根据化学方程式计算与化合价知识综合运用能力,难度较大.

练习册系列答案
相关题目
18.某有机物其结构如图所示,下列说法中正确的是( )
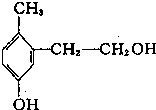

| A. | 它是苯酚的同系物 | |
| B. | 1mol有机物能与2molNaOH反应 | |
| C. | 1 mol该有机物能与金属钠反应产生O.5molH2 | |
| D. | 1 mol该有机物能与溴水反应消耗2 mol Br2发生取代反应 |
19.下列“油”中属于酯类的是( )
①豆油 ②酱油 ③牛油 ④甘油 ⑤重油 ⑥硝化甘油.
①豆油 ②酱油 ③牛油 ④甘油 ⑤重油 ⑥硝化甘油.
| A. | ①③⑥ | B. | ②④⑤ | C. | ①③④ | D. | ③⑤⑥ |
16.下列不能用作喷泉实验的组合的是( )
| A. | HCl和水 | B. | 氨气和稀硫酸 | ||
| C. | 氯气和饱和食盐水 | D. | CO2和NaOH溶液 |
3.三聚氰胺又名蛋白精[分子式:C3N3(NH2)3,相对分子质量:126]是一种低毒性化工产品,婴幼儿大量摄入可引起泌尿系统疾患.有关三聚氰胺的下列说法正确的是( )
| A. | 2.52 g三聚氰胺含氮原子数目为0.12NA | |
| B. | 标准状况下1 mol的三聚氰胺的体积为22.4 L | |
| C. | 三聚氰胺含氮量约为10% | |
| D. | 三聚氰胺的摩尔质量为126 |
13.食品安全已是百姓最关心的问题之一,食品在油炸过程中会产生一种不利于人体健康的物质CH2=CH-CO-NH2(丙烯酰胺),对这种物质的叙述不正确的是( )
| A. | 能发生加聚反应生成高分子化合物 | B. | 该物质与HCl加成产物只一种 | ||
| C. | 具有多种同分异构体 | D. | 可与强酸反应 |
20.下列物质中既能发生氧化反应,又能发生还原反应的是( )
| A. | 甲醇 | B. | 乙酸 | C. | 甲醛 | D. | 乙酸乙酯 |
18.能正确表示下列反应的离子方程式是( )
| A. | Cl2与水的反应:Cl2+H2O=2H++Cl-+ClO- | |
| B. | H2SO4与Ba(OH)2反应:Ba2++SO42-=BaSO4 | |
| C. | 铁溶于足量稀硝酸:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O | |
| D. | AlCl3溶液中加入过量稀氨水:Al3++3NH3•H2O=Al(OH)3+3NH4+ |