题目内容
反应A→C分两步进行:①A→B,②B→C。反应过程能量变化曲线如图所示(E1、E2、E3、E4表示活化能)。下列说法正确的是
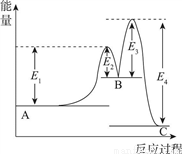
A. 两步反应的ΔH均大于0 B. 加入催化剂能改变反应的焓变
C. 三种物质中C最稳定 D. A→C反应的ΔH=E4-E1
练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
80 ℃时,2 L 密闭容器中充入0.40 mol N2O4,发生反应N2O4 2NO2 △H=+Q kJ·mol-1(Q>0),获得如下数据:下列判断正确的是
2NO2 △H=+Q kJ·mol-1(Q>0),获得如下数据:下列判断正确的是
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
c(NO2)/mol·L-1 | 0.00 | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
A. 升高温度该反应的平衡常数K减小
B. 20~40 s 内,v(N2O4)=0.002 mol/L .s
C. 反应达平衡时,吸收的热量为0.30 Q kJ/mol
D. 100s 时再通入0.40 mol N2O4,达新平衡时N2O4的转化率减小


