题目内容
10.下列变化中,需要加入氧化剂才能实现的是( )| A. | KCl→AgCl | B. | Cl2→NaClO | C. | SiO2→Si | D. | Cu→CuSO4 |
分析 需要加入氧化剂才能实现,则选项中为还原剂的氧化反应,还原剂中某元素的化合价升高,以此来解答.
解答 解:A.可与硝酸银反应实现,为复分解反应,故A错误;
B.可与氢氧化钠反应实现,为氯气的自身氧化还原反应,故B错误;
C.Si元素化合价降低,应加入还原剂,故C错误;
D.Cu元素化合价升高,被氧化,应加入氧化剂,故D正确.
故选D.
点评 本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重氧化剂、还原剂反应的考查,题目难度不大.

练习册系列答案
相关题目
20.下列说法错误的是( )
| A. | 钠在空气中燃烧最后所得产物为Na2O2 | |
| B. | 镁因在空气中形成了一层致密的氧化膜,保护了里面的镁,故镁不需要进行特殊保护 | |
| C. | 铝制品在生活中非常普遍,这是因为铝不活泼 | |
| D. | 铁在潮湿的空气中因为生成的氧化膜很疏松不能保护内层金属,故铁制品往往需涂保护层 |
1.C、H、O三种元素组成的T、X在一定条件下可以发生如下转化: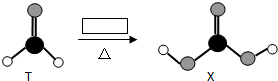
X不稳定,易分解.为使转化能够成功进行,方框内可能加入的试剂是( )

X不稳定,易分解.为使转化能够成功进行,方框内可能加入的试剂是( )
| A. | O2 | B. | NaOH溶液 | C. | 稀硫酸 | D. | Na2SO3溶液 |
18.常温下,0.1mol/L的氯化铵溶液中,下列描述及关系不正确的是( )
| A. | 溶液呈酸性 | |
| B. | c(NH3•H2O)+c(NH4+)=0.1mol/L | |
| C. | c(NH4+)+c(H+)=c(OH-)+c(Cl-) | |
| D. | 氯化铵的加入可抑制水的电离,使Kw=1.0×10-14 |
5.如图下列表述不正确的是( )
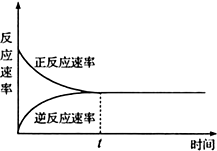

| A. | t时刻表示在给定条件下该反应在达到最大限度 | |
| B. | t时刻表示该反应达到化学平衡状态 | |
| C. | t时刻以前正反应速率大于逆反应速率 | |
| D. | t时刻及以后正反应速率等于逆反应速率等于0 |
15.下列叙述正确的是( )
| A. | 含有金属元素的离子一定是阳离子 | |
| B. | 金属阳离子被还原,一定得到金属单质 | |
| C. | 有单质参与的化合反应一定是氧化还原反应 | |
| D. | 在氧化还原反应中,非金属单质一定是氧化剂 |
2.23g金属钠投入足量水中,反应后生成的气体在标准状况体积为( )
| A. | 22.4 L | B. | 11.2 L | C. | 2 L | D. | 2.5L |
19.对于Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H<0 的化学反应,下列叙述错误的是( )
| A. | 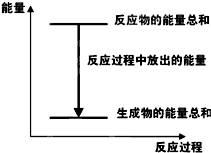 反应过程中能量关系可用如图表示 | |
| B. | 若将该反应设计成原电池则锌为负极 | |
| C. | △H的值与反应方程式的化学计量数有关 | |
| D. | 若将其设计为原电池,当有32.5g锌溶解时,转移电子数为2NA |
9.下列说法不正确的是( )
| A. | 同系物的化学性质相似 | |
| B. | 同位素的化学性质几乎相同 | |
| C. | 相对分子质量相同的化合物,互称同分异构体 | |
| D. | 同素异形体之间的转化,同分异构体之间的转化都属于化学变化 |