题目内容
【题目】下列关于Na2O和Na2O2的叙述正确的是( )
A.Na2O与Na2O2均可与水反应生成氢氧化钠,所以都是碱性氧化物
B.Na2O与Na2O2分别与CO2反应的产物完全相同
C.常温下,钠在空气中反应生成过氧化钠
D.在呼吸面具中,Na2O2常作供氧剂
【答案】D
【解析】
A.过氧化钠和水反应生成氢氧化钠和氧气,不属于碱性氧化物,故错误;
B.氧化钠和二氧化碳反应生成碳酸钠,过氧化钠和二氧化碳反应生成碳酸钠和氧气,故错误;
C.常温下,钠在空气中反应生成氧化钠,故错误;
D.过氧化钠能和水或二氧化碳反应生成氧气,所以可以做呼吸面具的供氧剂,故正确。
故选D。

【题目】Ⅰ.下表是元素周期表的一部分,根据表中列出的10种元素,回答下列问题。
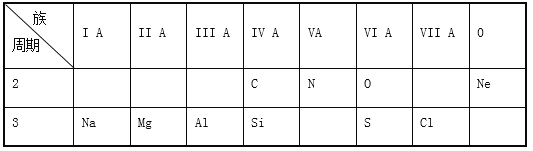
(1)O和S中,原子半径较大的是________;(填元素符号或化学,以下同)
(2)CH4和NH3中,热稳定性较强的是________;
(3)新制氯水有漂白作用,是因为其中含有________;
(4)元素最高价氧化物对应水化物中,两性氢氧化物是________________;
(5)上表元素中,存放最高价氧化物对应水化物的碱性最强的溶液的试剂瓶盖不能用玻璃塞,请写出该反应的离子方程式_______________。
Ⅱ.现有部分元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第3周期元素的简单离子中半径最小 |
(1)元素T在元素周期表中的位置是________________。
(2)元素Y与元素Z相比,金属性较强的是______(用元素符号表示),下列表述中能证明这一事实的是______(填序号)。
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈
d.Y最高价氧化物的水化物的碱性比Z强
(3)上述四种元素中有2种元素能形成一种淡黄色的固体,该化合物的电子式是________________,所含化学键的类型有________________。