题目内容
(8分)已知甲元素是第三周期p区元素,其最低氧化值为-1,乙元素是第四周期d区元素,其最高氧化值为+4,试填下表:
| 元素 | 价电子构型 | 族 | 金属或非金属 | 电负性相对高低 |
| 甲 | | | | |
| 乙 | | | | |
| 元素 | 价电子构型 | 族 | 金属或非金属 | 电负性相对高低 |
| 甲 | 3s23p5 | ⅦA | 非金属 | 较高 |
| 乙 | 4s23d2 | ⅣB | 金属 | 较低 |
甲:第三周期p区元素,最低氧化值-1,则最高氧化值+7,为Cl;乙:第四周期d区元素,最高氧化值+4,则电子构型4s23d2。元素为Ti。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
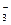 、Cl-
、Cl-