题目内容
K35ClO3与K37Cl在酸性溶液中反应生成氯气,则该氯气的相对分子质量为( )
| A.70.7 | B.71.0 | C.72.0 | D.73.3 |
D
K35ClO3与K37Cl在酸性溶液中发生氧化还原反应生成氯气。
(35Cl—37Cl):35ClO-3+37Cl?+H+→35Cl37Cl+H2O
根据电子转移守恒有:
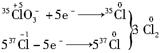
取生成的Cl23 mol,其中必含1 mol35Cl和5 mol37Cl,则氯气的摩尔质量为:
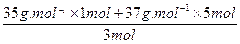 =73.3g·mol-1,氯气的相对分子质量为73.3,故选D项。
=73.3g·mol-1,氯气的相对分子质量为73.3,故选D项。
(35Cl—37Cl):35ClO-3+37Cl?+H+→35Cl37Cl+H2O
根据电子转移守恒有:
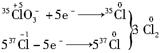
取生成的Cl23 mol,其中必含1 mol35Cl和5 mol37Cl,则氯气的摩尔质量为:
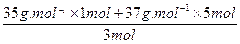 =73.3g·mol-1,氯气的相对分子质量为73.3,故选D项。
=73.3g·mol-1,氯气的相对分子质量为73.3,故选D项。
练习册系列答案
相关题目