题目内容
取标准状况下CH4和过量O2的混合气体840mL,点燃,将燃烧后的气体用过量碱石灰吸收,碱石灰增重0.600g。计算:
(1)碱石灰吸收后所剩气体的体积(标准状况下)。
(2)原混和气体中CH4跟O2的体积比。
【答案】
(1)336ml (2)1︰4
【解析】
试题分析:(1) 设原混合气体中CH4的物质的量为x
根据CH4燃烧的化学方程式可知
1molCH4完全燃烧得到的CO2和H2O共80g
则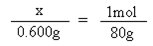
解得x=0.0075mol
所以CH4的体积为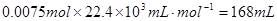
1molCH4完全燃烧需消耗2molO2
因此剩余气体的体积=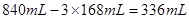
(2)根据(1)可知,氧气的体积是840ml-168ml=672ml
所以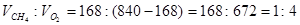
考点:考查甲烷燃烧的有关计算
点评:本题是中等难度的试题,试题基础性强,难易适中。有利于培养学生的规范答题能力,以及灵活运用知识解决实际问题的能力,有利于提高学生的学习效率。

练习册系列答案
相关题目