题目内容
【题目】下图为铜锌原电池的装置图,根据装置图填写空白.
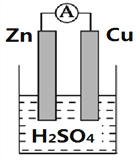
(1)将________转化为________的装置叫做原电池
(2)Zn极上的电极反应式为:_____________________________________。
(3)Cu极发生的是_____________反应(“氧化”或“还原”)。铜片上观察到的现象为___________________;
(4)溶液中H+的流动方向为__________________;
(5)若烧杯中溶液为AgNO3溶液,则负极为________(填Zn或Cu),总反应方程式为________________________________。
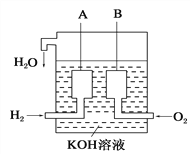
(6)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示:A、B两个电极均由多孔的碳块组成。该电池的正极反应物为:___________。
【答案】 化学能 为电能 Zn - 2e- = Zn2+ 还原 有气泡产生 由Zn极流向Cu极或从左到右 Zn Zn +2AgNO3=2Ag +Zn(NO3) 2 O2
【解析】(1)将化学能转化为电能的装置叫做原电池;(2)Zn的金属性强于铜,锌是负极,电极反应式为Zn - 2e- = Zn2+。(3)Cu极是正极,发生的是得到电子的还原反应,氢离子放电产生氢气,因此铜片上观察到的现象为有气泡产生;(4)溶液中的H+向正极铜电极移动;(5)若烧杯中溶液为AgNO3溶液,则负极仍然是锌,正极是铜,溶液中的银离子放电,总反应方程式为Zn +2AgNO3=2Ag +Zn(NO3) 2。(6)氧气在反应中得到电子,所以该电池的正极反应物为O2。

练习册系列答案
相关题目