题目内容
为了证明一水合氨(NH3·H2O)是弱电解质,甲、乙、丙三人分别选用下列试剂进行实验:
0.010 mol·L-1氨水、0.1 mol·L-1 NH4Cl溶液、NH4Cl晶体、酚酞试液、pH试纸、蒸馏水。
(1)甲用pH试纸测出0.010 mol·L-1氨水的pH为10,则认定一水合氨是弱电解质,你认为这一方法是否正确? (填“正确”或“不正确”),并说明理由 。
(2)乙取出10 mL 0.010 mol·L-1氨水,用pH试纸测其pH=a,然后用蒸馏水稀释至1 000 mL,再用pH试纸测其pH=b,若要确认NH3·H2O是弱电解质,则a、b应满足什么关系? 。
(3)丙取出10 mL 0.010 mol·L-1氨水,滴入2滴酚酞试液,显粉红色,再加入少量NH4Cl晶体,溶液颜色变 (填“深”或“浅”)。你认为这一方法能否证明NH3·H2O是弱电解质? (填“能”或“否”),并说明原因 。
(4)请你根据所提供的试剂,再提出一个合理又简便的方案证明NH3·H2O是弱电解质: 。
0.010 mol·L-1氨水、0.1 mol·L-1 NH4Cl溶液、NH4Cl晶体、酚酞试液、pH试纸、蒸馏水。
(1)甲用pH试纸测出0.010 mol·L-1氨水的pH为10,则认定一水合氨是弱电解质,你认为这一方法是否正确? (填“正确”或“不正确”),并说明理由 。
(2)乙取出10 mL 0.010 mol·L-1氨水,用pH试纸测其pH=a,然后用蒸馏水稀释至1 000 mL,再用pH试纸测其pH=b,若要确认NH3·H2O是弱电解质,则a、b应满足什么关系? 。
(3)丙取出10 mL 0.010 mol·L-1氨水,滴入2滴酚酞试液,显粉红色,再加入少量NH4Cl晶体,溶液颜色变 (填“深”或“浅”)。你认为这一方法能否证明NH3·H2O是弱电解质? (填“能”或“否”),并说明原因 。
(4)请你根据所提供的试剂,再提出一个合理又简便的方案证明NH3·H2O是弱电解质: 。
(1)正确 若是强电解质,则0.010 mol·L-1氨水中c(OH-)应为0.010 mol·L-1,pH=12
(2)a-2<b<a
(3)浅 能 0.010 mol·L-1氨水(滴有酚酞试液)中加入氯化铵晶体后颜色变浅,有两种可能:一是氯化铵在水溶液中电离出的NH4+水解使溶液显酸性,加入氨水中使其pH降低;二是NH4+使NH3·H2O的电离平衡NH3·H2O NH4++OH-逆向移动,从而使溶液的pH降低。这两种可能均可证明NH3·H2O是弱电解质
NH4++OH-逆向移动,从而使溶液的pH降低。这两种可能均可证明NH3·H2O是弱电解质
(4)取一张pH试纸,再用玻璃棒蘸取0.1 mol·L-1 NH4Cl溶液,滴在pH试纸上,显色后跟标准比色卡比较测出pH,pH<7(方案合理即可)
(2)a-2<b<a
(3)浅 能 0.010 mol·L-1氨水(滴有酚酞试液)中加入氯化铵晶体后颜色变浅,有两种可能:一是氯化铵在水溶液中电离出的NH4+水解使溶液显酸性,加入氨水中使其pH降低;二是NH4+使NH3·H2O的电离平衡NH3·H2O
 NH4++OH-逆向移动,从而使溶液的pH降低。这两种可能均可证明NH3·H2O是弱电解质
NH4++OH-逆向移动,从而使溶液的pH降低。这两种可能均可证明NH3·H2O是弱电解质(4)取一张pH试纸,再用玻璃棒蘸取0.1 mol·L-1 NH4Cl溶液,滴在pH试纸上,显色后跟标准比色卡比较测出pH,pH<7(方案合理即可)
(1)若NH3·H2O是强电解质,则0.010 mol·L-1氨水中c(OH-)应为0.010 mol·L-1,pH=12。用pH试纸测出0.010 mol·L-1氨水的pH为10,说明NH3·H2O没有完全电离,应为弱电解质。
(2)若NH3·H2O是强电解质,用蒸馏水稀释至1 000 mL,其pH=a-2。因为NH3·H2O是弱电解质,不能完全电离,a、b应满足a-2<b<a。
(3)向0.010 mol·L-1氨水中加入少量NH4Cl晶体,有两种可能:一是氯化铵在水溶液中电离出的NH4+水解使溶液显酸性,加入氨水中使其pH降低;二是NH4+使NH3·H2O的电离平衡NH3·H2O NH4++OH-逆向移动,从而使溶液的pH降低。这两种可能均会使溶液颜色变浅,可证明NH3·H2O是弱电解质。
NH4++OH-逆向移动,从而使溶液的pH降低。这两种可能均会使溶液颜色变浅,可证明NH3·H2O是弱电解质。
(4)NH4Cl为强酸弱碱盐,只需检验NH4Cl溶液的酸碱性,即可证明NH3·H2O是弱电解质,还是强电解质。
(2)若NH3·H2O是强电解质,用蒸馏水稀释至1 000 mL,其pH=a-2。因为NH3·H2O是弱电解质,不能完全电离,a、b应满足a-2<b<a。
(3)向0.010 mol·L-1氨水中加入少量NH4Cl晶体,有两种可能:一是氯化铵在水溶液中电离出的NH4+水解使溶液显酸性,加入氨水中使其pH降低;二是NH4+使NH3·H2O的电离平衡NH3·H2O
 NH4++OH-逆向移动,从而使溶液的pH降低。这两种可能均会使溶液颜色变浅,可证明NH3·H2O是弱电解质。
NH4++OH-逆向移动,从而使溶液的pH降低。这两种可能均会使溶液颜色变浅,可证明NH3·H2O是弱电解质。(4)NH4Cl为强酸弱碱盐,只需检验NH4Cl溶液的酸碱性,即可证明NH3·H2O是弱电解质,还是强电解质。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
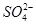
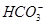
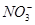 、
、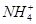 、Fe2+、Cl-
、Fe2+、Cl-
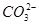
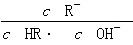 相等(HR代表CH3COOH或HClO)
相等(HR代表CH3COOH或HClO) H++A2-
H++A2-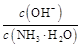 增大
增大