题目内容
16.下列说法正确的是( )| A. | NaHCO3分解过程中,只需克服离子键 | |
| B. | Na2O溶于水的过程中破坏了离子键和共价键,形成了新的离子键和共价键 | |
| C. | O3、CO2和SiO2都是由分子构成的 | |
| D. | 金刚石和足球烯(C60)均为原子晶体,沸点极髙 |
分析 A、NaHCO3分解生成碳酸钠、水和二氧化碳;
B、Na2O溶于水时与水反应生成氢氧化钠,破坏了Na2O中的离子键和水中共价键,生成氢氧化钠时形成了新的离子键和共价键;
C、SiO2是由原子构成的原子晶体;
D、足球烯(C60)为分子晶体.
解答 解:A、NaHCO3分解生成碳酸钠、水和二氧化碳,所以克服离子键和共价键,故A错误;
B、Na2O溶于水时与水反应生成氢氧化钠,破坏了Na2O中的离子键和水中共价键,生成氢氧化钠时形成了新的离子键和共价键,故B正确;
C、SiO2是由原子构成的原子晶体,故C错误;
D、足球烯(C60)为分子晶体,沸点低,故D错误;
故选B.
点评 本题考查晶体类型及化学键,明确不同类型的晶体在发生变化时克服不同的作用力是解答本题的关键,题目难度不大,注意把握晶体类型.

练习册系列答案
相关题目
7.中国古代涉及化学的叙述,下列解读错误的是( )
| A. | 《黄白第十六》中“曾青涂铁,铁赤如铜”'其“曾青”是铜盐 | |
| B. | 《汉书》中“高奴县有淆水可燃中的淆水指的是石油 | |
| C. | 《天工开物》中“凡石灰,经火焚炼为用”里的“石灰”指的是Ca(OH)2 | |
| D. | 《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的碱是碳酸钾 |
4.化学生活密切相关,下列说法正确的是( )
| A. | 淀粉纤维素和油脂都属于天然高分子化合物 | |
| B. | 汽车尾气污染物中含有氮的氧化物,主要是汽油不完全燃烧造成成的 | |
| C. | 盐卤点豆腐,明矾净水和利用电泳来分离各种氨基酸和蛋白质都与胶体的性质有关 | |
| D. | 尽量使用含12C的产品,减少使用含13C或14C的产品符合“促进低碳经济”宗旨 |
11.下列属于弱电解质的是( )
| A. | NH3•H2O | B. | CuSO4 | C. | Ba(OH)2 | D. | 酒精 |
1.下列物质中只含离子键的是( )
| A. | MgCl2 | B. | NaOH | C. | HC1 | D. | CH3COONa |
8.下列物质中,属于天然有机高分子化合物的是( )
| A. | 葡萄糖 | B. | 蔗糖 | C. | 淀粉 | D. | 塑料 |
5.下列化学用语表示正确的是( )
| A. | HClO的结构式:H-Cl-O | B. | NH4Cl的电子式为: | ||
| C. | CO2的比例模型: | D. | 甲烷的球棍模型: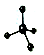 |
8.下列说法正确的是( )
| A. | 只含有非金属元素的化合物一定是共价化合物 | |
| B. | NaOH、H2SO4溶于水均克服了离子键 | |
| C. | CO2、PCl3中所有原子最外层都满足8电子结构 | |
| D. | 金刚石和足球烯都属于原子晶体,熔化只克服共价键 |