题目内容
【题目】现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。A元素的价电子构型为nsnnpn+1;C元素为最活泼的非金属元素,D元素核外有三个电子层,最外层电子数是核外电子总数的1/6;E元素正三价离子的3d轨道为半充满状态,F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)A元素的第一电离能________B元素的第一电离能(填“<”“>”或“=”)。
(2)D元素基态原子核外电子占据的最高能层符号为________, DC2的电子式为__________。
(3)E原子价电子的轨道表示式为_____________________________。
(4)F其基态原子的电子排布式为_____________________,元素位于元素周期表的_______区。
(5)G元素可能的性质是___________(填序号)。
A.其单质可作为半导体材料
B.其电负性大于磷
C.最高价氧化物对应的水化物是强酸
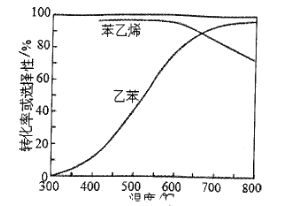
(6)含A、B等元素的化合物的结构如图1所示,该化合物中含有_________(填序号)。
a.极性共价键 b.非极性共价键 c.配位键 d.氢键 e.金属键
(7)A和E形成的一种化合物的晶胞结构如图2所示,该晶胞的化学式为_____________。若两个最近的E原子间的距离为acm,则该晶体的密度是________________g·cm-3。(用NA和a表示)
【答案】 > M ![]()
![]() 1s22s22p63s23p63d104s1 或 [Ar]3d104s1 ds A abcd Fe4N
1s22s22p63s23p63d104s1 或 [Ar]3d104s1 ds A abcd Fe4N ![]()
【解析】A元素的价电子构型为nsnnpn+1,n=2,A为N元素,C元素为最活泼的非金属元素,C为F元素,则B为O元素,D元素核外有三个电子层,最外层电子数是核外电子总数的1/6,应为Mg元素,E元素正三价离子的3d轨道为半充满状态,则原子序数为26,为Fe元素,F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,为Cu元素,G元素与A元素位于同一主族,其某种氧化物有剧毒,为As元素;则
(1)N原子最外层为半充满状态,性质稳定,难以失去电子,第一电离能大于O元素;(2)D为Mg元素,基态原子核外电子占据的最高能层符号为M, MgF2是离子化合物,电子式为![]() ;(3)E为Fe元素,价电子的轨道表示式为
;(3)E为Fe元素,价电子的轨道表示式为![]() ;(4)F为Cu,位于周期表ds区,其基态原子的电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1;(5)A、G为As元素,与Si位于周期表对角线位置,其单质可作为半导体材料,A正确;B、同主族从上到下电负性逐渐减小,电负性比P小,B错误;C、因磷酸为中强酸,则As的最高价氧化物对应的水化物是弱酸,C错误,答案选A;(6)根据结构图可知不同的非金属原子之间存在极性键、C和C之间存在非极性键,氧原子和氢原子之间还存在氢键,另外N和Ni之间还存在配位键,不存在金属键,答案选abcd;(7)铁和氮形成的晶体的晶胞结构如图所示,晶胞中铁原子数目为8×1/8+6×1/2=4,氮原子数目为1,原子数目之比为4:1,故该氯化物的化学式是Fe4N,晶胞质量为 238/NAg,若两个最近的Fe原子间的距离为acm,则该晶体的晶胞边长为
;(4)F为Cu,位于周期表ds区,其基态原子的电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1;(5)A、G为As元素,与Si位于周期表对角线位置,其单质可作为半导体材料,A正确;B、同主族从上到下电负性逐渐减小,电负性比P小,B错误;C、因磷酸为中强酸,则As的最高价氧化物对应的水化物是弱酸,C错误,答案选A;(6)根据结构图可知不同的非金属原子之间存在极性键、C和C之间存在非极性键,氧原子和氢原子之间还存在氢键,另外N和Ni之间还存在配位键,不存在金属键,答案选abcd;(7)铁和氮形成的晶体的晶胞结构如图所示,晶胞中铁原子数目为8×1/8+6×1/2=4,氮原子数目为1,原子数目之比为4:1,故该氯化物的化学式是Fe4N,晶胞质量为 238/NAg,若两个最近的Fe原子间的距离为acm,则该晶体的晶胞边长为![]() ,则该晶体密度为
,则该晶体密度为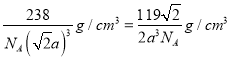 。
。

【题目】苯甲酸乙酯(C9H10O2)稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为:
已知:
颜色、状态 | 沸点(℃) | 密度(g·cm-3) | 相对分子质量 | |
苯甲酸* | 白色片状晶体 | 249 | 1.2659 | 122 |
苯甲酸乙酯 | 无色澄清液体 | 212.6 | 1.05 | 150 |
乙醇 | 无色澄清液体 | 78.3 | 0.7893 | 46 |
环己烷 | 无色澄清液体 | 80.8 | 0.7318 | 84 |
*苯甲酸在 100℃会迅速升华。

实验步骤如下:
①在 100mL 圆底烧瓶中加入 12.20g 苯甲酸、25mL乙醇(过量)、20mL 环己烷,以及 4mL浓硫酸,混合均匀并加入沸石,按右图所示装好仪器,并在分水器中预先加入水,使水面略低于分水器的支管口,控制温度在 65~70℃加热回流 2h。反应时环己烷-乙醇-水会形成“共沸物”(沸点62.6℃)蒸馏出来。在反应过程中,通过分水器下部的旋塞分出生成的水,注意保持分水器中水层液面原来的高度,使油层尽量回到圆底烧瓶中。
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞。继续加热,至分水器中收集到的液体不再明显增加,停止加热。
③将烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性。
④用分液漏斗分出有机层,水层用 25mL 乙醚萃取分液,然后合并至有机层。加入氯化钙,对粗产物进行蒸馏,低温蒸出乙醚后,继续升温,接收 210—213℃的馏分。
⑤检验合格,测得产品体积为 11.43mL。
回答下列问题:
(1)装置 X 的作用是_________;进水口为_________(a或者b)。
(2)步骤①中使用分水器不断分离除去水的目的是_________。
(3)步骤②中应控制馏分的温度在_________。
A.65~70℃ B.78~80℃ C.85~90℃ D.215~220℃
(4)若 Na2CO3加入不足,在步骤④蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是_________。
(5)该实验的产率为_________。
【题目】某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。
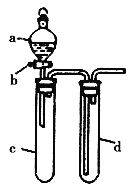
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,其目的是_____________________。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸,c中反应的化学方程式是______________________________________________。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是____________。
方案 | 反应物 |
甲 | Cu、浓HNO3 |
乙 | Cu、稀HNO3 |
丙 | Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明酸性:HCl>H2CO3>H2SiO3,则分液漏斗a中加入的试剂是____________,c中加入的试剂是____________,d中加入的试剂是____________,实验现象为____________________________________________。有同学认为,该实验装置仍不能证明上述结论,改进的措施是_________________________________________。