题目内容
【题目】关于如图所示装置的判断,叙述正确的是( )
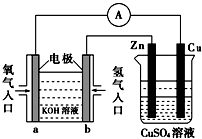
A.左边的装置是电解池,右边的装置是原电池
B.该装置中铜为正极,锌为负极
C.当铜片的质量变化为12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L
D.装置中电子的流向是:a→Cu→经过CuSO4溶液→Zn→b
【答案】C
【解析】
试题分析:左边的装置是氢氧燃料电池,b通入氢气发生氧化反应是原电池的负极,a是正极;左边的装置是氢氧燃料电池,右边是电解池,故A错误;该装置中铜与正极相连,是电解池阳极,锌与负极相连,是阴极,故B错误;根据电子守恒,![]() ,当铜片的质量变化为12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L,故C正确;溶液中没有电子流动,装置中电子的流向是:b→Zn;Cu→a,故D错误。
,当铜片的质量变化为12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L,故C正确;溶液中没有电子流动,装置中电子的流向是:b→Zn;Cu→a,故D错误。

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
【题目】某原电池的离子方程式是 Zn + Cu2+ = Zn2+ + Cu,该原电池正确的组成是 ( )
正极 | 负极 | 电解质溶液 | |
A. | Cu | Zn | HCl |
B. | Zn | Cu | CuSO4 |
C. | Cu | Zn | CuSO4 |
D. | Cu | Zn | ZnCl2 |
A. A B. B C. C D. D