题目内容
【题目】亚磷酸钠(Na2HPO3)溶液电渗析法制备 H3PO3(亚磷酸)的原理如图所示,下列有关说法不正确的是
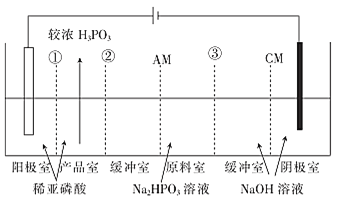
CM:阳离子交换膜,只允许阳离子透过
AM:阴离子交换膜,只允许阴离子透过
A.膜①、②、③均为CM
B.阴极的电极反应式为2H2O+2e-= 2OH- +H2↑
C.阳极的电极反应式为2H2O-4e-= 4H+ +O2↑
D.在原料室与产品室间设计缓冲室的主要目的是提高产品的纯度
【答案】A
【解析】
电解池中阳离子要有流向阴极的趋势,阴离子有流向阳极的趋势。
A.阳极室发生4OH-+4e-=O2↑+2H2O,水的电离平衡被破坏,产生大量的氢离子,氢离子需要迁移到产品室,则膜①为阳离子交换膜(CM);原料室的HPO32-需要迁移扩散至产品室,则膜②为阴离子交换膜(AM);为防止过多OH-迁移到产品室,所以膜③为阳离子交换膜(CM),故A错误;
B.在阴极上氢离子得电子发生还原反应,电极反应式为2H++2e-=H2↑,或写为:2H2O+2e-=2OH-+H2↑,故B正确;
C.在阳极上氢氧根失电子发生氧化反应,电极方程式为4OH-+4e-=O2↑+2H2O,或写为2H2O-4e-= 4H+ +O2↑,故C正确;
D.若无缓冲室,大量氢氧根进入产品室,会降低产品的纯度,故D正确;
故答案为A。

练习册系列答案
相关题目