题目内容
【题目】利用电溶氧化法从低品位钼矿中回收铼(Re),其原理如图所示,下列说法正确的是
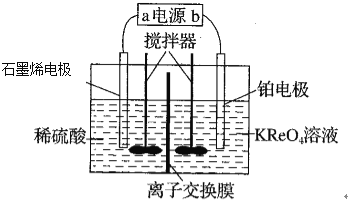
A.阴极材料选用石墨烯增大了接触面积
B.上图装罝中的离子交换膜为阴离子交换膜
C.铂电极反应式为8H++ReO4-+7e-=Re+4H2O
D.有0.4mole-转移时,石墨烯上产生0.2mo1H2
【答案】C
【解析】
根据题意,利用电溶氧化法从低品位钼矿中回收铼(Re),因此右侧ReO4-得到电子,发生还原反应,铂电极为阴极,电极方程式为ReO4-+7e-+8H+=Re+4H2O;而石墨烯电极为阳极,稀硫酸中的H2O失去电子,生成O2,电极方程式为2H2O-4e-=4H++O2↑。
A.选用石墨烯,可以增大接触面积,但是根据分析,石墨烯电极为电解池的阳极,而不是阴极,A错误;
B.在电解池的右侧,ReO4-得到电子生成Re,电极方程式为ReO4-+7e-+8H+=Re+4H2O;电解池的左侧,稀硫酸中的H2O失去电子,电极方程式为2H2O-4e-=4H++O2↑,左侧生成的H+,经过离子交换膜到达右侧被消耗;右侧溶液中的K+也需要移动到左侧,与SO42-结合,因此该离子交换膜为阳离子交换膜,B错误;
C.根据分析,铂电极为阴极,ReO4-得到电子生成Re,发生还原反应,电极方程式为ReO4-+7e-+8H+=Re+4H2O,C正确;
D.根据分析,石墨烯电极为阳极,稀硫酸中的H2O失去电子,生成O2,电极方程式为2H2O-4e-=4H++O2↑,不产生H2,D错误。
答案选C。

练习册系列答案
相关题目