题目内容
同温同压下,某容器充满O2重116 g,若充满CO2重122 g,现充满某气体重114 g,则该气体的相对分子质量为A.28 B.60 C.32 D.44
A
解析:方法一:按常规思路,设瓶重m g。该气体的摩尔质量为M,则![]() ,因为容器体积不变,所以有
,因为容器体积不变,所以有![]() ,得m=100,然后由
,得m=100,然后由![]() ,得M=28 g·mol-1,即相对分子质量为28,选A。
,得M=28 g·mol-1,即相对分子质量为28,选A。
方法二:差量法:由气体定律可知同温同压下,气体质量之差和相对分子质量之间存在着正比关系,因此可以不计算容器的质量,直接由气体质量差和相对分子质量差的正比关系求得。即![]() ,M=28 g·mol-1Mr=28
,M=28 g·mol-1Mr=28
方法三:估算法:由阿伏加德罗定律可知n(O2)=n(CO2)=n(气体),m=n·M,m与M成正比。
故M(气)<M(O2),M(气)<M(CO2),即M(气)<32 g·mol-1,选A。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
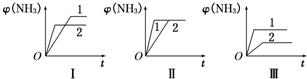
 2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.
2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.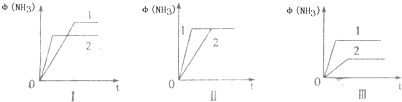
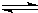 H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发
H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发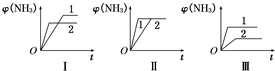 合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响.合成氨反应的化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ?mol-1.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷或焦炭与水蒸气反应制得.
合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响.合成氨反应的化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ?mol-1.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷或焦炭与水蒸气反应制得.