��Ŀ����
����Ŀ��25��ʱ��������Һ�е���Ũ�ȹ�ϵ��ȷ����
A. pH = 3 ��0.1 molL-1��NaHC2O4��Һ�У�c(H+ )=c(OH-)+c(C2O42-)
B. 0.1 molL-1��(NH4)2S��Һ����c(NH4+)=2c(S2-)+2c(HS-)+2c(H2S)
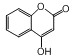
C. pH = 4 �� CH3COOH ��Һ�У�![]() <1
<1
D.�����ʵ���Ũ�ȡ��������NaF��Һ��HF��Һ�������ϡ��Һ����c(H+ )+ C(HF)<c(F-) + 2c(OH-)
���𰸡�D
��������A�NaHC2O4��Һ�У����ڵ���غ�������غ㣬���������غ��c��Na+��=c��HC2O4-��+c��H2C2O4��+c��C2O42-�������ݵ���غ��c��H+��+c��Na+��=c��HC2O4-��+2c��C2O42-��+c��OH-�������Ե�c��H+��+c��H2C2O4��=c��C2O42-��+c��OH-�����ʴ���B����������غ㣺c��NH3��H2O��+c(NH4+)=2c(S2-)+2c(HS-)+2c(H2S)������C�CH3COOH ��Һ�У�![]() =[c��CH3COO-����c��H+��]/[c��CH3COOH����Kw]=Ka/Kw������Ka>Kw��
=[c��CH3COO-����c��H+��]/[c��CH3COOH����Kw]=Ka/Kw������Ka>Kw��![]() >1������D���������ʵ���Ũ�ȡ��������NaF��Һ��HF��Һ�������ϡ��Һ�У����ݵ���غ㣺c��Na+��+c��H+��=c��OH-��+c��F-���������غ㣺2c��Na+��=c��HF��+c��F-����c��HF��+2c��H+��= c��F-��+2 c��OH-������c(H+ )+ C(HF)<c(F-) + 2c(OH-)����ȷ��
>1������D���������ʵ���Ũ�ȡ��������NaF��Һ��HF��Һ�������ϡ��Һ�У����ݵ���غ㣺c��Na+��+c��H+��=c��OH-��+c��F-���������غ㣺2c��Na+��=c��HF��+c��F-����c��HF��+2c��H+��= c��F-��+2 c��OH-������c(H+ )+ C(HF)<c(F-) + 2c(OH-)����ȷ��

 ��Ӣ���㿨ϵ�д�
��Ӣ���㿨ϵ�д� Ӧ����㲦ϵ�д�
Ӧ����㲦ϵ�д�����Ŀ���Ƽ��仯������й㷺����;��
��1�������£�Ũ�Ⱦ�Ϊ0.1mol/L����������������Һ��pH���±���
���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
��������Һ�е������ӣ����������������ǿ���� �����ݱ������ݣ�Ũ�Ⱦ�Ϊ0.01mol/L���������������Һ�ֱ�ϡ��100����pH�仯������ �����ţ���
A��HCN B��HClO C��CH3COOH D��H2CO3
��2���Т�100mL0.1mol/L̼������ ��100mL0.1mol/L̼����������Һ����Һ��ˮ������������Ӹ�����
�� �� ���>����=����<����ͬ������Һ�������ӵ����ʵ���Ũ��֮�ͣ��� �ڡ�
��3��̼��������һ�� ���ǿ�����������������д��HCO3-ˮ������ӷ���ʽ�� �������£�0.1mol/L̼��������Һ��pH����8������Һ��Na+��HCO3-��H2CO3��CO32-��OH-��������Ũ���ɴ�С��˳��Ϊ�� ��
��4��ʵ�����г�����������������ϴ�����ᴿ��
�ٵ�150mL1mol/L������������Һ���ձ����2.24L������̼ʱ��������Һ�и�����Ũ���ɴ�С��˳��Ϊ�� ��
�� �������ӿ�ʼ����ʱ��pH���±���
���� | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
������ͬŨ�ȵ�Cu2+��Mg2+��Fe2+����Һ�еμ�����������Һʱ�� (�����ӷ���)�ȳ�����Ksp[Fe(OH)3]
Ksp[Mg(OH)2] ���>����=����<������Ҫʹ0.2mol/L����ͭ��Һ��ͭ���ӳ�����Ϊ��ȫ��ʹͭ����Ũ�Ƚ���ԭ����ǧ��֮һ������Ӧ����Һ���������������Һʹ��ҺpHΪ ��
( Ksp[Cu(OH)2]=2��10-20mol2/L2)
����Ŀ��CaCO3��ϡ���ᷴӦ�����и���ʵ���У���Ӧ��������һ����(����)
��� | �¶ȣ����� | CaCO3��״̬ | ϡ����Ũ�ȣ�mol/L�� |
A | 20 | ��״ | 1 |
B | 30 | ��״ | 1 |
C | 30 | ��״ | 2 |
D | 30 | ��״ | 2 |
A. A B. B C. C D. D