题目内容
【题目】下列说法不正确的是( )
A. 三聚氰酸(C3H3N3O3)的结构式为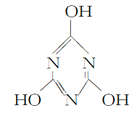 ,它属于共价化合物
,它属于共价化合物
B. 只含H、N、O三种元素的化合物,可能是离子化合物,也可能是共价化合物
C. NaHCO3、CH3COONa均含有离子键和共价键
D. 化合物MgO、H2O中化学键的类型相同
【答案】D
【解析】A. 三聚氰酸(C3H3N3O3)的结构式为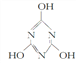 ,其中不存在离子键,属于共价化合物,故A正确;B、H、N、O三种元素的化合物中,硝酸铵是离子化台物,硝酸是共价化合物,所以可能是离子化含物,也可能是共价化合物,故B正确;C、NaHCO3中氢、碳、氧之间是以共价键结合,而钠离子与碳酸氢根离子的离子键结合,CH3COONa中氢、碳、氧之间是以共价键结合,而钠离子与醋酸根离子之间是离子键结合,所以两者中均含有离子键和共价键,故C正确;D、MgO是离子键,而H2O中存在共价键,所以化学键类型不同,故D错误;故选D。
,其中不存在离子键,属于共价化合物,故A正确;B、H、N、O三种元素的化合物中,硝酸铵是离子化台物,硝酸是共价化合物,所以可能是离子化含物,也可能是共价化合物,故B正确;C、NaHCO3中氢、碳、氧之间是以共价键结合,而钠离子与碳酸氢根离子的离子键结合,CH3COONa中氢、碳、氧之间是以共价键结合,而钠离子与醋酸根离子之间是离子键结合,所以两者中均含有离子键和共价键,故C正确;D、MgO是离子键,而H2O中存在共价键,所以化学键类型不同,故D错误;故选D。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目