��Ŀ����
����Ŀ����һ���¶��£�������X������Y��0.16mol����10L�����ܱ������У�������ӦX(g)+Y(g) ![]() 2Z(g) ��H<0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
2Z(g) ��H<0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
t/min | 2 | 4 | 7 | 9 |
N(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
����˵����ȷ����
A. ��Ӧǰ2min��ƽ������v(Z)=2.0��10-5 mol��L-1��min-1
B. ���¶��´˷�Ӧ��ƽ�ⳣ��K=1.44
C. �����������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰv���棩��v������
D. �����������䣬�ٳ���0.2 mol Z��ƽ��ʱX�������������
���𰸡�B
�����������ݷ���ʽ�� ��Ӧǰ2min����Z�����ʵ���0.08mol�� ![]() 4.0��10-3mol��L-1��min-1����A�����ݡ�����ʽ����
4.0��10-3mol��L-1��min-1����A�����ݡ�����ʽ����
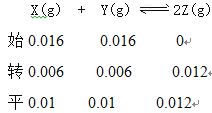
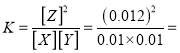 1.44����B��ȷ�������������䣬�����¶ȣ�ƽ�������ƶ�����Ӧ�ﵽ��ƽ��ǰv���棩<v����������C���������������䣬�ٳ���0.2molZ�����൱������ѹǿ��ƽ��ʱX������������䣬��D����
1.44����B��ȷ�������������䣬�����¶ȣ�ƽ�������ƶ�����Ӧ�ﵽ��ƽ��ǰv���棩<v����������C���������������䣬�ٳ���0.2molZ�����൱������ѹǿ��ƽ��ʱX������������䣬��D����

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
