��Ŀ����
�±����������ڲ�ͬ�¶��µ��ܽ�ȣ�g/100gˮ����
| | NaNO3 | KNO3 | NaCl | KCl |
| 10�� | 80.5 | 21.2 | 35.7 | 31.0 |
| 100�� | 175 | 246 | 39.1 | 56.6 |
�����裺�����ʱ��Ӱ����Ե��ܽ�ȣ����뾧��ʱ���ܼ�����ĺ��Բ��ƣ�
ijͬѧ��������ʵ���֮��Ϊ1��1�������ƺ��Ȼ���Ϊԭ�ϣ�����һ������ˮ��ȡ����ص�ʵ�飬����������ͼ��ʾ��

��1���ڢٺ͢ڵ�ʵ������У���Ҫ���ƵĹؼ���ʵ��������______________________�������������У�______���A����C����ӦΪ����ؾ��塣
��2���ڢٵ�ʵ������У���Ҫ���еIJ���������________________��________________��_____________��
��3���ֲ�Ʒ�п��ܺ�����������_______________________����������һ�����ӵķ�����________________________________________________________________________��
��4��Ϊ��ϴ�����õ�����ؾ��壬�����ܼ�������ϴ�Ӽ�����___________�����ţ���
a����ˮ b����ˮ c��95%�ľƾ� d�����Ȼ�̼
��5����ȡ34.0g�����ƺ�29.8g�Ȼ��أ�����70gˮ����100��������50gˮ��ά�ָ��¶ȣ����ˣ��������������Ϊ_______________��
��1���¶ȣ� C ��1�֣�
��2����ˮ�ܽ⡢����Ũ�������ȹ���
��3��Na+��Cl¯�� �ýྻ�IJ�˿����˿պȡ�ֲ�Ʒ�ڻ��������գ�������ʻ�ɫ��֤����Na+���� ȡ�ֲ�Ʒ��������ˮ�����Һ�����������ữ����������Һ�����а�ɫ����������֤����Cl¯����2�֣�
��4��bc ��2�֣�
��5��15.6g ��2�֣�
���������������1����ˮ�м��������NaNO3��KCl����Һ���е�����Na+��NO3����K+��Cl��������������Ͽɵõ����е�4�����࣬���ݱ������ݣ���������������ˮ�е��ܽ�������¶ȵ����߶����ߣ�������KNO3 ���¶������ܽ�ȼ����������Ҫ����Һ�з����KNO3 Ӧ�ÿ����¶���ʵ�ַ��룬��Ϊʵ��Ŀ���ǵõ�����ؾ��壬��˾���C����Ŀ����
��2��Ҫ�õ�����ؾ��壬Ӧ������NaCl���¶ȱ仯�ܽ�ȱ仯����KNO3 ���¶������ܽ�ȼ���������ص㣬��ʵ�鲽��1���Ȱѹ����ܽ⣬Ȼ������Ũ������ʱNaCl���¶ȱ仯�ܽ�ȱ仯�����Ծ�����ʽ���������Գ��ȹ��ˣ������KNO3 ��������ҺB�У�Ȼ���ٶ���ҺB����Ũ����ȴ�ᾧ��KNO3 �ܽ�ȼ����С�������壬�ٹ��˿ɵ�KNO3 ���塣
��3�����ڸı��¶ȱ�Ȼ����������NaClҲ����ڴֲ�ƷKNO3 �����У���˺���Na+��Cl¯�������ӣ�����ķ���������ɫ��Ӧ���������ӣ����������Լ����������ӡ�
��4��ϴ�Ӳ�Ʒԭ�����ܹ���ϴ���������ӵ�����ͬʱ�������ٲ�Ʒ����ʧ������Ӧ���������¶ȵ͵�ϴ�Ӽ����߲�Ʒ���ܵ����ʿ��ܵ�ϴ�Ӽ��������ۺϿ���Ӧѡbc��
��5������100�����������Һ��NaClΪ������Һ��KNO3Ϊ��������Һ�����Ը����ܽ�ȶ���
100��������50.0��H2O����Һ��NaCl������Ϊ ���ֳ�ʼ���������Ϊ
���ֳ�ʼ���������Ϊ �������൱��n(NaCl)=0.4mol,��m��(NaCl)=0.4mol��58.5g/mol=23.4g������������NaCl��23.4g��7.82g=15.6g��
�������൱��n(NaCl)=0.4mol,��m��(NaCl)=0.4mol��58.5g/mol=23.4g������������NaCl��23.4g��7.82g=15.6g��
���㣺���⿼��������ʵķ��뷽���ؽᾧ�Լ��ܽ�ȵ����⡣

ij��ѧʵ���Ҳ����ķ�Һ�к���Fe3����Cu2����Ba2����Cl���������ӣ���������з����Է�Һ���д������Ի��ս������Ʊ��Ȼ������Ȼ������塣
��1������1�к��еĽ��������� ��
��2������ʱ����H2O2��Һ������Ӧ�����ӷ���ʽΪ ��
��3�����������У�������Ϊ�Լ�X���� ������ĸ����
| A��BaCl2 | B��BaCO3 |
| C��NaOH | D��Ba(OH)2 |
��5���Ʊ��Ȼ�������������豣�������������Ŀ���� ��
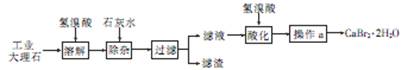
��6���ɹ���2�õ�����Һ�Ʊ�BaCl2��ʵ���������Ϊ ����ȴ�ᾧ�� ��ϴ�ӡ����
Ϊ̽��ij����ҩX����ɣ���������ʵ�飺
�������ϣ�
�ٿ���ҩX���ܵ���ɿ��Ա�ʾΪ��MgmAln(OH)p(CO3)q(SiO3)r��m��n��p��q��rΪ��0����������
�� ��pH=5.0ʱ������ȫ��
��pH=5.0ʱ������ȫ�� ��pH=8.8ʱ��ʼ������pH=11.4ʱ������ȫ��
��pH=8.8ʱ��ʼ������pH=11.4ʱ������ȫ��
ʵ����̣�
| ���� | ʵ����� | ʵ������ |
| I | ��X�ķ�ĩ�м���������� | ��������A���õ���ɫ��Һ |
| II | ������õ���Һ�еμӰ�ˮ������pH��5~ 6������ | ���ɰ�ɫ����B |
| III | �����B�мӹ���NaOH��Һ | ����ȫ���ܽ� |
| IV | ��II�õ�����Һ�еμ�NaOH��Һ������pH��12 | ���ɰ�ɫ����C |
��1����������A��ʹ����ʯ��ˮ����ǣ�A�Ļ�ѧʽ�� ��
��2��II������B��Ӧ�����ӷ���ʽ�� ��
��3��III��B�ܽⷴӦ�����ӷ���ʽ�� ��
��4������C�Ļ�ѧʽ�� ��
��5��������n(A)�Un(B)�Un(C)=1�U2�U3����X�Ļ�ѧʽ�� ��
ѡ������ʵ�鷽���������ʣ������뷽����������ں����ϡ�
| A����ȡ��Һ | B������ | C���ᾧ | D����Һ E������ F������ G������ |
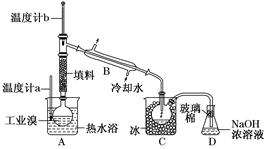
��2��__ _������غ��Ȼ��ƵĻ��Һ�л������ء�
��3��__ _����ˮ�����͵Ļ���
��4��__ _����CCl4���е�Ϊ76.75�棩�ͼױ����е�Ϊ110.6�棩�Ļ���
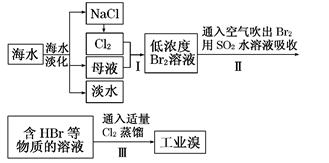
���������һ������Ч���ˮ����������ҵ�ϳ�����NaClO��������������Ӧԭ��Ϊ��
���ڼ��������£�����NaClO����Fe(NO3)3�Ƶ�Na2FeO4
3NaClO + 2Fe(NO3)3 + 10NaOH��2Na2FeO4��+ 3NaCl + 6NaNO3 + 5H2O
��Na2FeO4��KOH��Ӧ����K2FeO4��Na2FeO4 + 2KOH��K2FeO4 + 2NaOH
��Ҫ�������������£�
��1���������������ҺpHʱ����pH��ֽ���Բ���pH�Կ��Ƽ������������ʵ������pH��ֽ�ⶨ��ҺpH�IJ����� ��
��2������ͼ�С�ת��������Ӧ�ۣ�����ij�����½��еģ�˵�����¶���Ksp��K2FeO4�� Ksp��Na2FeO4���������������������
��3����Ӧ���¶ȡ�ԭ�ϵ�Ũ�Ⱥ���ȶԸ�����صIJ��ʶ���Ӱ�졣
ͼ1Ϊ��ͬ���¶��£�Fe(NO3)3��ͬ����Ũ�ȶ�K2FeO4�����ʵ�Ӱ�죻
ͼ2Ϊһ���¶��£�Fe(NO3)3����Ũ�����ʱ��NaClOŨ�ȶ�K2FeO4�����ʵ�Ӱ�졣
��ҵ����������¶�Ϊ �棬��ʱFe(NO3)3��NaClO������Һ�������Ũ��֮��Ϊ ��
��4��K2FeO4��ˮ��Һ���ס�ˮ�⡱��4FeO42- + 10H2O  4Fe(OH)3 + 8OH- + 3O2���ڡ��ᴿ��K2FeO4�в����ؽᾧ��ϴ�ӡ����º�ɵķ�������ϴ�Ӽ����ѡ�� ��Һ������ţ���
4Fe(OH)3 + 8OH- + 3O2���ڡ��ᴿ��K2FeO4�в����ؽᾧ��ϴ�ӡ����º�ɵķ�������ϴ�Ӽ����ѡ�� ��Һ������ţ���
| A��H2O | B��CH3COONa������� | C��NH4Cl������� | D��Fe(NO3)3������� |