题目内容
15.下列叙述中,错误的是( )| A. | 乙烷与氯气在光照下反应只生成一氯乙烷 | |
| B. | 苯在合适条件下催化加氢可生成环己烷 | |
| C. | 乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷 | |
| D. | 苯与浓硝酸、浓硫酸共热并保持50-60℃反应生成硝基苯 |
分析 A.光照下乙烷中H可被取代;
B.苯可与氢气发生加成反应;
C.乙烯中含双键,可与溴发生加成反应;
D.苯中的H可发生取代反应.
解答 解:A.光照下乙烷中H可被取代,为链锁反应,乙烷与氯气在光照下反应生成一氯乙烷、二氯乙烷、三氯乙烷等,故A错误;
B.苯可与氢气发生加成反应,则苯在合适条件下催化加氢可生成环己烷,故B正确;
C.乙烯中含双键,可与溴发生加成反应,则乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷,故C正确;
D.苯中的H可发生取代反应,则苯与浓硝酸、浓硫酸共热并保持50-60℃反应生成硝基苯,故D正确;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重常见有机物性质及分析与应用能力的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.羟基是重要的官能团.某化学小组以下列4种物质的溶液做研究对象,比较不同物质的羟基中氢原子的活泼性.
①碳酸 ②乙醇 ③苯酚 ④乙酸
Ⅰ甲同学设计并实施了如下实验方案.
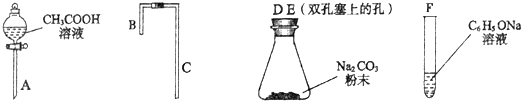
Ⅱ乙同学在研究了甲同学的实验方案后,提出如下改进方案,能一次比较乙酸、碳酸和苯酚的羟基中氢原子的活泼性,实验仪器如图所示.
利用上述仪器组装实验装置,其中A管插入(填字母,下同)D(或E)中,B管插入E(或D)中,C管插入F中.
Ⅲ丙同学认为乙同学的实验设计不完善,请说明不完善的理由因乙酸有挥发性,制得的CO2中含有乙酸,如何改正才能使乙同学的实验设计更加完善,请说明在试管F之前增加了一个盛有饱和NaHCO3溶液的洗气装置.
①碳酸 ②乙醇 ③苯酚 ④乙酸
Ⅰ甲同学设计并实施了如下实验方案.
| 编号 | 实验操作 | 实验现象 | 结论及解释 |
1 | 分别取4中溶液,滴加紫色石蕊溶液 | 溶液变红的是① ④溶液 | 略 |
2 | 向含酚酞的NaOH溶液中,各滴加等量②③两 | ②中无明显现象 ③中红色明显变浅 | 滴加③时反应的化学的化学方程式: |
| 3 | 测定CH3COOH溶液 与H2CO3溶液的溶液的酸性 | 略 | CH3COOH溶液的酸性远大于H2CO3溶液 |
| 4 | 将CO2通入C6H5ONa溶液中 | 反应的化学方程式: | |
| 结论:由强到弱顺序(填序号) | |||
利用上述仪器组装实验装置,其中A管插入(填字母,下同)D(或E)中,B管插入E(或D)中,C管插入F中.
Ⅲ丙同学认为乙同学的实验设计不完善,请说明不完善的理由因乙酸有挥发性,制得的CO2中含有乙酸,如何改正才能使乙同学的实验设计更加完善,请说明在试管F之前增加了一个盛有饱和NaHCO3溶液的洗气装置.

6.1mol钠、镁、铝分别与200mL2mol/L的盐酸反应,下列说法正确的是( )
| A. | 三种金属产生氢气的量相同 | |
| B. | 钠反应生成的氢气的量最多 | |
| C. | 铝反应产生的氢气的量最多 | |
| D. | 钠、镁与酸反应生成的氢气的量相同 |
3.已知:乙烯是一种无色稍有气味气体,难溶于水,易溶于四氯化碳等有机溶剂:SO2易溶于水,难溶于四氯化碳等有机溶剂.实验室制乙烯时,产生的气体能使溴水褪色,甲、乙同学探究溴水褪色的原因.(气密性已检验,部分夹持装置略).
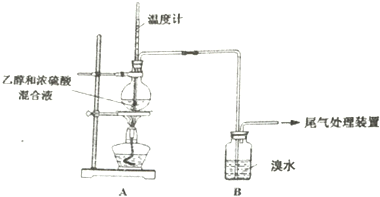
(1)写出生成乙烯的化学方程式CH3-CH2-OH $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O.烧瓶内液体渐渐变黑说明浓硫酸具有脱水性、强氧化 性.
(2)分析使B中溶液褪色的物质,甲认为是C2H4,乙认为不能排除SO2的作用.
①根据甲的观点,C2H4使B中溶液褪色的化学方程式为CH2=CH2+Br2→CH2Br-CH2Br.
②乙根据现象c认为产生了SO2,SO2使B中溶液褪色的化学方程式是SO2+Br2+2H2O=2HBr+H2SO4.
(3)为证实各自观点,甲、乙同学重新实验,各自在A、B间增加一个装有某种试剂的洗气瓶,均观察到溴水褪色.
①根据甲的设计,洗气瓶中盛放的试剂是NaOH溶液.
②乙为进一步验证其观点,取少量反应后的B中溶液,加入少量BaCl2溶液,振荡,产生大量白色沉淀,反应的离子方程式为SO2+2H2O+Br2═4H++2Br-+SO42-、SO42-+Ba2+═BaSO4↓或SO2+2H2O+Br2+Ba2+═4H++2Br-+BaSO4↓.

| 操作 | 现象 |
| 点燃酒精灯, 加热至170℃ | a.A中烧瓶内液体渐渐变黑 b.B内气泡连续冒出,溶液逐渐褪色 |
| … | |
| 实验完毕 | c.A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(2)分析使B中溶液褪色的物质,甲认为是C2H4,乙认为不能排除SO2的作用.
①根据甲的观点,C2H4使B中溶液褪色的化学方程式为CH2=CH2+Br2→CH2Br-CH2Br.
②乙根据现象c认为产生了SO2,SO2使B中溶液褪色的化学方程式是SO2+Br2+2H2O=2HBr+H2SO4.
(3)为证实各自观点,甲、乙同学重新实验,各自在A、B间增加一个装有某种试剂的洗气瓶,均观察到溴水褪色.
①根据甲的设计,洗气瓶中盛放的试剂是NaOH溶液.
②乙为进一步验证其观点,取少量反应后的B中溶液,加入少量BaCl2溶液,振荡,产生大量白色沉淀,反应的离子方程式为SO2+2H2O+Br2═4H++2Br-+SO42-、SO42-+Ba2+═BaSO4↓或SO2+2H2O+Br2+Ba2+═4H++2Br-+BaSO4↓.
10.100g浓度为18mol/L密度为ρg/mL的浓硫酸中加入一定的水稀释成9mol/L的硫酸,则加入水的体积为( )
| A. | 小于100mL | B. | 等于100mL | C. | 大于100mL | D. | 等于100/ρmL |
20.关于如图所示装置的叙述,正确的是( )
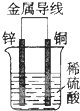

| A. | 铜片为负极 | B. | 铜片质量逐渐减少 | ||
| C. | 电子从锌片经导线流向铜片 | D. | 氢离子在铜片表面被氧化 |
7.在碱性溶液中,能大量共存的离子组是( )
| A. | Mg2+?SO42-?K+?Cl- | B. | K+?Cl-?NO-3?Cu2+ | ||
| C. | Na+?SO2-4?H+?NO-3 | D. | K+?CO32-?Cl-?Na+ |