题目内容
【题目】尿素[CO(NH2)2]是首个由无机物人工合成的有机物。
(1)工业上用CO2和NH3在一定条件下合成,其反应方程式__________。
(2)在一个2L的密闭容器内,当起始投入量氨碳比![]() =4,CO2的转化率随时间的变化关系如下图所示。
=4,CO2的转化率随时间的变化关系如下图所示。
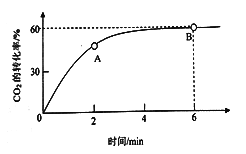
① A点的逆反应速率v逆(CO2) __________________B点的正反应速率为v正(CO2)(填“大于”、“小于”或“等于”)
②假设氨的起始投入量为8mol,求从开始到达到平衡状态这段时间内v(NH3)=_________________。
③NH3的平衡转化率为____________________。
④单纯从制备的成本角度考虑,我们希望氨碳比![]() 尽可能__________(“大”、“小”)因为_________。
尽可能__________(“大”、“小”)因为_________。
【答案】 2NH3+CO2═CO(NH2)2+H2O 小于 v(NH3)=0.2 mol/(L·min) NH3的平衡转化率为30% 氨碳比![]() 尽可能小 因为可以提高价格较高的NH3的转化率
尽可能小 因为可以提高价格较高的NH3的转化率
【解析】(1)CO2和NH3合成CO(NH2)2,根据元素守恒可知,同时还有H2O生成,化学方程式为:2NH3+CO2![]() CO(NH2)2+H2O;
CO(NH2)2+H2O;
(2)①由CO2的转化率随时间变化图可知在A点时反应还未达到平衡状态,反应仍将继续正向进行,故v逆(CO2)小于B点平衡时的化学反应速率;
②假设氨的起始投入量为8mol,则CO2的投入量为2mol,平衡时CO2的转化率为60%,CO2的变化量为1.2mol,NH3的变化量为2.4mol,达到平衡状态这段时间内v(NH3)=![]() =0.2 mol/(L·min);
=0.2 mol/(L·min);
③设CO2的初始物质的量为a,则NH3的初始物质的量为4a,由图可知,CO2的转化率为60%,故转化的二氧化碳为a×60%=0.6a,根据方程式可知,转化的NH3的物质的量为0.6a×2=1.2a,故平衡时氨气的转化率定为![]() ×100%=30%;
×100%=30%;
④增加一种反应物,可促进平衡正向移动,提高另一种反应物的转化率,即氨碳比![]() 尽可能小,可以提高价格较高的NH3的转化率。
尽可能小,可以提高价格较高的NH3的转化率。