题目内容
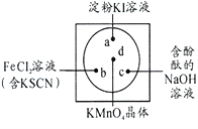
【题目】高锰酸钾溶液在酸性条件下可以与硫酸亚铁反应,化学方程式如下(未配平):KMnO4+FeSO4+H2SO4―→K2SO4+MnSO4+Fe2(SO4)3+H2O。下列说法正确的是
A. Fe2+的还原性强于Mn2+
B. MnO4-是氧化剂,Fe3+是还原产物
C. 生成1 mol水时,转移1.25 mol电子
D. 取反应后的溶液加KSCN溶液,可观察到有血红色沉淀生成
【答案】AC
【解析】
A.该反应中还原剂是Fe2+,还原产物是Mn2+,还原剂的还原性大于还原产物的还原性,故A正确;B.该反应中,锰元素的化合价由+7价变为+2价,铁元素的化合价由+2价变为+3价,所以氧化剂是MnO4-,还原产物是Mn2+,故B错误;C.根据得失电子相等配平方程式得2KMnO4+10FeSO4+8H2SO4=K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,根据方程式知,生成1mol水时,转移电子的物质的量=![]() =1.25mol,故C正确;D.铁离子和硫氰化钾溶液反应生成络合物而没有沉淀,故D错误;故选AC。
=1.25mol,故C正确;D.铁离子和硫氰化钾溶液反应生成络合物而没有沉淀,故D错误;故选AC。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目