题目内容
【题目】下列依据所给条件推出的结论不正确的是( )
选项 | 条件 | 结论 |
A | 在水溶液中或熔融状态下可以导电的化合物称为电解质 | CH3COOH水溶液中存在:CH3COOH |
B | 凡是能给出质子的分子或离子称为酸,凡是能接受质子的分子或离子称为碱 | H2O既是酸又是碱 |
C | Fe3Cl8可以改写为FeCl2·2FeC13 | Fe3I8可以改写为FeI·2FeI3 |
D | HCl在一定条件下能被MnO2氧化为Cl2 | HBr在一定条件下也能被MnO2氧化为Br2 |
A.AB.BC.CD.D
【答案】C
【解析】
A. 醋酸在水溶液中可以部分电离,溶液中有自由移动的离子,能导电,是电解质,A正确;
B. H2O![]() H++OH-,水即可以电离出H+,又可以电离出+OH-,所以H2O即为酸又为碱,B正确;
H++OH-,水即可以电离出H+,又可以电离出+OH-,所以H2O即为酸又为碱,B正确;
C. Fe3+与I-发生氧化还原反应生成. Fe2+和I2,所以不存在FeI3,Fe3I8可以改写为3FeI2·I2,C错误;
D. HBr的还原性强于HCl,HCl在一定条件下能被MnO2氧化为Cl2,HBr在一定条件下也能被MnO2氧化为Br2,D正确;故答案为:C。

 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案【题目】某学习小组通过下列装置探究MnO2与FeCl36H2O能否反应产生Cl2。
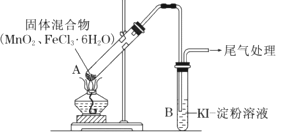
资料:FeCl3是一种共价化合物,熔点306℃,沸点315℃。
ⅰ.实验操作和现象:
操作 | 现象 |
点燃酒精灯,加热 | i.A中部分固体溶解,上方出现白雾 ii.稍后,产生黄色气体,管壁附着黄色液滴 iii.B中溶液变蓝 |
ⅱ.分析现象的成因:
(1)现象i中的白雾是______,用化学方程式和必要的文字说明白雾的形成原因是______。
(2)分析现象ii,该小组探究黄色气体的成分,实验如下:
a.直接加热FeCl3·6H2O,产生白雾和黄色气体。
b.将现象ii和a中的黄色气体通入KSCN溶液,溶液均变红。通过该实验说明现象ii中黄色气体含有______。
(3)除了氯气可使B中溶液变蓝外,该小组还提出其他两种可能的原因:
可能原因①:实验b检出的气体使之变蓝;
反应的离子方程式是______。
可能原因②:______;
反应的离子方程式是______。
(4)为进一步确认黄色气体中是否含有Cl2,小组提出两种方案,均证实了Cl2的存在。
方案1 | 在A、B间增加盛有某种试剂的洗气瓶C | B中溶液变为蓝色 |
方案2 | 将B中KI-淀粉溶液替换为NaBr溶液;检验Fe2+ | B中溶液呈浅橙红色;未检出Fe2+ |
①方案1的C中盛放的试剂是______,从化学平衡原理的角度加以解释______。
②方案2中检验Fe2+的最佳试剂是______,若存在Fe2+,则现象是______。
③综合方案1、2的现象,说明方案2中选择NaBr溶液的依据是______。
(5)将A中产物分离得到Fe2O3和MnCl2,A中产生Cl2的化学方程式是______。
【题目】FTO导电玻璃为抄杂氟的SnO2透明导电玻璃,r泛用于液晶显示屏,薄膜太阳能电池基底等方面,SnCl4可用于制作FTO导电玻璃。实验室可用熔融的锡与Cl2反应制备SnCl4,此反应放热,生成的SnCl4易水解生成SnO2XH2O。回答下列问题:

有关物理性质如下表:
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
Sn | 银白色固体 | 231.9 | 2260 |
SnCl4 | 无色液体 | -33 | 114 |
SnCl2 | 无色晶体 | 246 | 652 |
(1)将上述装置用玻璃管连接,组装成一套制备SnCl4的实验装置(每个装置最多使用一次),正确的顺序是:(填各接口的字母)
B →____ →____ →____ →____→_____N→A→____ →___→____→____;
(2)Ⅲ处中应选用的冷凝管为_______(填选项字母);

(3)检查装置气密性并装好药晶后,应先______待出现______再点燃I处的酒精灯,否则会有副反应发生:①___________________.②_________________(用化学方程式表示);
(4)Cl2和锡的反应产物有SnCl4和SnCl2,为减少产晶中SnCl2的量,可采取的措施是_______________________________、____________________________________;
(5)已知Fe3++Sn2+—Fe2++Sn4+(未配平)。准确称取样品mg于饶杯中。用少量浓盐酸溶解。加入过量的氧化铁溶液,再加水稀释,配制成250 mL.溶液。取25.00 mL于锥形瓶中。用0.1000 mol·L-1 K2Cr2O7标准溶液滴定至终点,消耗标准液15.00 mL.则产品中SnCl2的含量W _______% (用含m的代数式表示)。
【题目】如图所示装置中观察到电流计指针偏转,M棒变粗、N棒变细,以此判断下表中所列M、N、P物质,其中可以成立的是

选项 | M | N | P |
A | 锌 | 铜 | 稀硫酸溶液 |
B | 铜 | 铁 | 稀盐酸溶液 |
C | 银 | 锌 | 硝酸银溶液 |
D | 锌 | 铁 | 硝酸铁溶液 |
A.AB.BC.CD.D