题目内容
下列反应的离子方程式不正确的是( )
| A、新制的氧化铝可溶于氢氧化钠溶液:Al2O3+2OH-=2AlO2-+H2O |
| B、二氧化硫通入次氯酸钠溶液:SO2+ClO-+2OH-=SO42-+Cl-+H2O |
| C、过量的NaHSO4和Ba(OH)2溶液反应:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
| D、在氢氧化钾的稀溶液中通少量的二氧化碳气体:CO2+2OH-═CO32-+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A、氧化铝是两性氧化物在氢氧化钠溶液中溶解生成偏铝酸钠和水;
B、二氧化硫具有还原性,次氯酸具有氧化性,二氧化硫被次氯酸氧化为硫酸;
C、酸式盐和碱反应,量少的全部反应;
D、少量二氧化碳通入氢氧化钾溶液反应生成碳酸钾和水.
B、二氧化硫具有还原性,次氯酸具有氧化性,二氧化硫被次氯酸氧化为硫酸;
C、酸式盐和碱反应,量少的全部反应;
D、少量二氧化碳通入氢氧化钾溶液反应生成碳酸钾和水.
解答:
解:A、氧化铝是两性氧化物在氢氧化钠溶液中溶解生成偏铝酸钠和水,氧化铝可溶于氢氧化钠溶液反应的离子方程式:Al2O3+2OH-=2AlO2-+H2O,故A正确;
B、二氧化硫具有还原性,次氯酸具有氧化性,二氧化硫被次氯酸氧化为硫酸,反应的离子方程式SO2+ClO-+2OH-=SO42-+Cl-+H2O,故B正确;
C、酸式盐和碱反应,量少的全部反应,过量的NaHSO4和Ba(OH)2溶液反应离子方程式:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故C错误;
D、少量二氧化碳通入氢氧化钾溶液反应生成碳酸钾和水,在氢氧化钾的稀溶液中通少量的二氧化碳气体反应的离子方程式:CO2+2OH-═CO32-+H2O,故D正确;
故选C.
B、二氧化硫具有还原性,次氯酸具有氧化性,二氧化硫被次氯酸氧化为硫酸,反应的离子方程式SO2+ClO-+2OH-=SO42-+Cl-+H2O,故B正确;
C、酸式盐和碱反应,量少的全部反应,过量的NaHSO4和Ba(OH)2溶液反应离子方程式:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故C错误;
D、少量二氧化碳通入氢氧化钾溶液反应生成碳酸钾和水,在氢氧化钾的稀溶液中通少量的二氧化碳气体反应的离子方程式:CO2+2OH-═CO32-+H2O,故D正确;
故选C.
点评:本题考查了离子方程式书写方法和正误判断,主要是氧化还原反应产物分析判断,量不同产物不同,掌握基础是关键.

练习册系列答案
相关题目
下列变化中,必须加入还原剂才能实现的是( )
| A、NaCl→AgCl |
| B、H2O→O2 |
| C、KClO3→KCl |
| D、MnO2→MnCl2 |
下列说法中正确的一组是( )
| A、正丁烷和异丁烷是同系物 |
| B、CH3CH2CH2CH(C2H5)CH3和C2H5CH(CH3)CH2CH2CH3是同一种物质 |
| C、H2和D2互为同位素 |
D、 和 和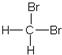 互为同分异构体 互为同分异构体 |
下列说法中正确的( )
A、
| ||||
| B、SO2和SO3属于同分异构体 | ||||
| C、正丁烷和异丁烷属于同分异构体 | ||||
| D、2H2和3H2属于不同的核素 |
与NH4+离子、质子总数和电子总数都相同的微粒是( )
| A、Al3+ |
| B、H3O+ |
| C、OH- |
| D、Na+ |
石灰氮是由Ca、N、C等三种元素组成的盐,其含钙、碳的质量分数分别为50%、l5%.
①石灰氮完全水解的产物是A和B,其中B可方便地制成一种氮肥;
②A在高温下分解生成C和D,通常状况下,C为气体;
③B的催化氧化产物为E和F;
④E遇到D生成唯一产物G,G与C反应重新生成A和E;
⑤F再被氧气氧化后的产物遇到E可制备常用的一种强酸H;
⑥B、C、E混合反应生成一种常用的氮肥I.
以下有关叙述中正确的是( )
①石灰氮完全水解的产物是A和B,其中B可方便地制成一种氮肥;
②A在高温下分解生成C和D,通常状况下,C为气体;
③B的催化氧化产物为E和F;
④E遇到D生成唯一产物G,G与C反应重新生成A和E;
⑤F再被氧气氧化后的产物遇到E可制备常用的一种强酸H;
⑥B、C、E混合反应生成一种常用的氮肥I.
以下有关叙述中正确的是( )
| A、石灰氮是化学式为Ca(CN)2 |
| B、②、⑤、⑥为有关工业生产过程的反应原理 |
| C、1mol B经过催化氧化生成E和F的过程中有3mol电子发生转移 |
| D、足量B和C与饱和氯化钠溶液反应可以制得发酵粉的一种主要成分 |
下列有关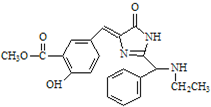 的说法中不正确的是( )
的说法中不正确的是( )
 的说法中不正确的是( )
的说法中不正确的是( )| A、该有机物能发生水解反应 |
| B、该有机物的化学式为C21H20N3O4 |
| C、该有机物不能发生消去反应 |
| D、该有机物既能与溴水反应,又能与碳酸钠溶液反应 |
铍元素性质与铝元素性质相似,下列方法能证明氯化铍由共价键构成的是( )
| A、溶于水加硝酸银溶液,观察是否有白色沉淀生成 |
| B、溶于水做导电实验,观察是否导电 |
| C、熔融状态,做导电实验,观察是否导电 |
| D、测定氯化铍熔点 |