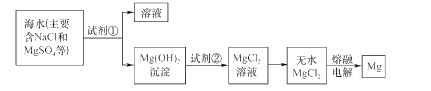
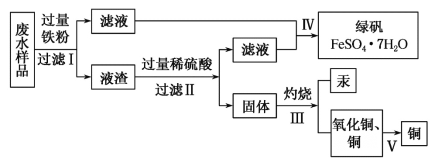
��Ŀ����
����Ŀ����Ҫ�����������գ�
��1�����и��������밴Ҫ�������գ�
��H��D ��O2��O3 ���������뻷���� ��C2H6��CH3CH2CH2CH3 ��C2H4��C3H6 ��CH2�TCHCH�TCH2��CH![]() CH ��Һ�������� ���Ȼ��������� ��
CH ��Һ�������� ���Ȼ��������� ��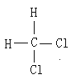 ��
��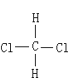 ��
��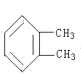 ��
��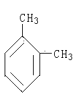
����ͬ�����������_______ ������ͬλ�ص���_________ ������ͬ�����ʵ���___________������ͬϵ�����__________ ��
��2��ij�л������ʽΪC5H12�����л��������ֻ��һ����ͬ��ѧ�������⣬�л���Ľṹ��ʽΪ___________��
���𰸡��� �� �ߢ�� �� 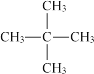
��������
��1��ͬ�������壺��ͬ��Ԫ����ɽṹ��ͬ�ĵ��ʣ�����ͬ�������嶨����Ǣڣ�
ͬλ�أ���������ͬ����������ͬͬ��Ԫ�ز�ͬԭ�ӵĻ��ƣ����϶�����Ǣ٣�
Һ��������Һ����õ��ģ����Һ������������ͬ�����ʣ��������Ȼ�������ˮ�����ڻ����Ȼ������ڴ��������Ȼ�����������ͬ�����ʣ�����Ŀռ乹��Ϊ�������壬���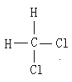 ��
��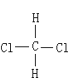 ����ͬ�����ʣ����ռ乹��Ϊƽ���������Σ�
����ͬ�����ʣ����ռ乹��Ϊƽ���������Σ�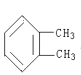 ��
��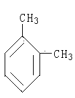 ����ͬ�����ʣ��������ͬ�����ʵ��Ǣߢ�⣻
����ͬ�����ʣ��������ͬ�����ʵ��Ǣߢ�⣻
ͬϵ���ǽṹ���ƣ�������������������CH2��ԭ���ŵ��л������ͬϵ����Ǣܣ�
��2�����л���ֻ��һ����ͬ��ѧ������H�������л���Ľṹ��ʽΪ ��
��

 ��������״Ԫ��ϵ�д�
��������״Ԫ��ϵ�д� �ƸԿ�����ҵ��ϵ�д�
�ƸԿ�����ҵ��ϵ�д� ��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
��Ԫ����ĩ��ϰ�ȷ��ϵ�д�����Ŀ����ҵ����N2��H2�ϳ�NH3���Ʊ�H2�辭�ಽ��ɣ�������ˮú����CO��H2���任���Ǵ���H2�Ĺؼ�һ����
��1��ˮú���任��CO��g��+ H2O��g��![]() CO2��g�� + H2��g�����÷�Ӧ��H = +41 kJ/mol����41 kJ/mol��
CO2��g�� + H2��g�����÷�Ӧ��H = +41 kJ/mol����41 kJ/mol��
�� ƽ�ⳣ��K���¶ȱ仯���£�
�¶�/�� | 200 | 300 | 400 |
K | 290 | 39 | 11.7 |
���з�����ȷ����__________��
a. ˮú���任��Ӧ��H��0
b. ����ѹǿ���������CO��ƽ��ת����
c. ����ˮ����Ũ�ȣ�����ͬʱ����CO��ƽ��ת���ʺͷ�Ӧ����
�� �¶�ΪT1ʱ�����ݻ�Ϊ2 L ���ܱ������ס����зֱ����һ������CO��H2O��g����
����������£�
���� | �� | �� | ||
��Ӧ�� | CO | H2O | CO | H2O |
��ʼʱ���ʵ�����mol�� | 1.2 | 0.6 | 2.4 | 1.2 |
ƽ��ʱ���ʵ�����mol�� | 0.8 | 0.2 | a | b |
�ﵽƽ���ʱ�䣨min�� | t 1 | t 2 | ||
��. �������У���Ӧ��t1 min �ڵ�ƽ����Ӧ����v��H2��=_____mol/��L��min����
��. �������У�ƽ��ʱ����Ӧ�������仯Ϊ_____kJ��
��. T1ʱ����Ӧ��ƽ�ⳣ��K��= ______��
��. ��������a =______mol��
��2����ˮΪ���ռ��ѳ�CO2������ʧȥ��������ʱ��ͨ������ʹ���ռ��������û�ѧ����ʽ��ʾ�����������̣�___________________________________��
��3��2016���ҹ�ij�����Ŷ�������Ĥ��һ�������N2��H2������ԭ����ͼ��ʾ����������N2��O2�����ʵ���֮�Ȱ�4:1�ƣ���
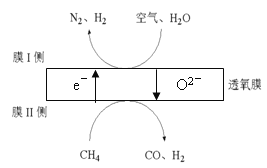
�� ��ԭ���õ�������_______��
�� Ĥ������ĵ缫��Ӧʽ��_______��
����Ŀ�������8�֣����в���Ԫ�ص�������ԭ��(�����)�ṹ���±���
Ԫ�ر�� | Ԫ��������ԭ��(�����)�ṹ |
T | �����������Ǵ�����������3�� |
X | �����µ���Ϊ˫ԭ�ӷ��ӣ������к���3�Թ��õ��Ӷ� |
Y | M���K����1������ |
Z | ��������Ԫ�صļ������а뾶��С |
(1)д��Ԫ��T��ԭ�ӽṹʾ��ͼ ��
(2)Ԫ��Y��Ԫ��Z��ȣ������Խ�ǿ����________(��Ԫ�ط��ű�ʾ)�����б�������֤����һ��ʵ����________(�����)��
a��Y���ʵ��۵��Z���ʵ�
b��Y�Ļ��ϼ۱�Z��
c��Y������ˮ��Ӧ��Z���ʾ���
d��Y����������ˮ����ļ��Ա�Zǿ
(3)T��X��Y��Z��������Ԫ�����γɼ������Ӽ����зǼ��Թ��ۼ��Ļ����д���û�����ĵ���ʽ��_____ _________��
(4)Ԫ��T����Ԫ�ؿ��γ�һ��18���ӵĻ�����Q��Ԫ��X����Ԫ��Ҳ�ܰ�ԭ�Ӹ�����Ϊ1��2�γ�һ��18���ӻ�����W��Q��W����������ԭ��Ӧ������X���ʺ�T����һ���⻯�д���÷�Ӧ�Ļ�ѧ����ʽ�� ��