题目内容
15. 有X、Y、Z三种物质,它们之间存在如图转化关系:
有X、Y、Z三种物质,它们之间存在如图转化关系:(1)若X、Y、Z三种物质的焰色反应均为黄色,三个反应均为化合反应,则Y的化学式为Na2O,Z的电子式为
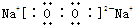 ;Y、Z两种物质相比,相同的化学键类型为离子键,当由X制取Z的上述两种途径生成Z的量相等时,转移电子数目比为1:2.
;Y、Z两种物质相比,相同的化学键类型为离子键,当由X制取Z的上述两种途径生成Z的量相等时,转移电子数目比为1:2.(2)若X、Y、Z均为常见化合物且三种物质中均含有相同的两种短周期元素,0.1mol/L的三种物质的溶液pH:Y>X>Z>7,则①的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
③的离子方程式为CO32-+CO2+H2O═2HCO3-.
(3)若X、Y、Z三种物质均含有同一种金属元素,X是单质,Y是日常生活中最重要的盐,②的反应条件为电解,则②的化学方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$ 2NaOH+H2↑+Cl2↑,
③的离子方程式为2Na+2H2O═2Na++2OH-+H2↑.
分析 (1)若X、Y、Z三种物质的焰色反应均为黄色,则应含有Na元素,三个反应均属于为化合反应,可知X为Na,Y为Na2O,Z为Na2O2;
(2)若X、Y、Z三种均为常见化合物且三种物质中均含有相同的两种短周期元素,0.1mol/L的三种物质的溶液pH:Y>X>Z>7,则Y是强碱,X、Z是强碱弱酸盐,其溶液呈碱性,又因为这三种物质为常见化合物且三种物质中均含有相同的两种短周期元素,所以Y是氢氧化钠,X是碳酸钠,Z是碳酸氢钠;
(3)若X、Y、Z三种物质均含有同一种金属元素,Y是日常生活中最重要的盐,则Y是氯化钠,X是单质,则X是钠,②的反应条件为电解,电解饱和氯化钠溶液生成氢氧化钠、氢气和氯气,Z中含有金属元素,则Z是氢氧化钠
解答 解:(1)若X、Y、Z三种物质的焰色反应均为黄色,则这三种物质都含有钠元素,三个反应均为化合反应,则Y中含有变价元素,根据教材知识知,X是钠、Y是氧化钠、Z是过氧化钠,通过以上分析知,Y是氧化钠,其化学式为Na2O,Z是过氧化钠,其电子式为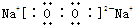 ,Y和Z中都含有离子键,但Z中还含有非极性共价键,当②、③两个反应生成的Z量相等时,分别发生:2Na2O+O2=2Na2O2,2Na+O2=Na2O2,若生成2molNa2O2,转移的电子的物质的量分别为2mol、4mol,
,Y和Z中都含有离子键,但Z中还含有非极性共价键,当②、③两个反应生成的Z量相等时,分别发生:2Na2O+O2=2Na2O2,2Na+O2=Na2O2,若生成2molNa2O2,转移的电子的物质的量分别为2mol、4mol,
则转移的电子数目之比为1:2,
故答案为:Na2O;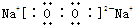 ;离子键;1:2;
;离子键;1:2;
(2)若X、Y、Z三种均为常见化合物且三种物质中均含有相同的两种短周期元素,0.1mol/L的三种物质的溶液pH:Y>X>Z>7,则Y是强碱,X、Z是强碱弱酸盐,其溶液呈碱性,又因为这三种物质为常见化合物且三种物质中均含有相同的两种短周期元素,所以Y是氢氧化钠,X是碳酸钠,Z是碳酸氢钠,
碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠,反应方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH,
碳酸钠和二氧化碳、水反应生成碳酸氢钠,离子反应方程式为:CO32-+CO2+H2O═2HCO3-,
故答案为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;CO32-+CO2+H2O═2HCO3-;
(3)若X、Y、Z三种物质均含有同一种金属元素,Y是日常生活中最重要的盐,则Y是氯化钠,X是单质,则X是钠,②的反应条件为电解,电解饱和氯化钠溶液生成氢氧化钠、氢气和氯气,反应方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,Z中含有金属元素,则Z是氢氧化钠,钠和水反应生成氢氧化钠和氢气,离子反应方程式为2Na+2H2O═2Na++2OH-+H2↑,
故答案为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;2Na+2H2O═2Na++2OH-+H2↑.
点评 本题考查无机物的推断,侧重于学生的分析能力和计算能力的考查,为高考常见题型,注意元素化合物知识的积累,把握常见物质的性质,难度中等

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
| A. | 高分子化合物 | B. | 芳香烃 | C. | 烃 | D. | 有机物 |
| 物质 | 杂质 | 试剂 | 方法 | |
| A | 二氧化碳 | 二氧化硫 | NaOH溶液 | 洗气 |
| B | 氯化亚铁溶液 | 氯化铁 | 过量铁粉 | 过滤 |
| C | 氧化铁 | 氧化铝 | 氨水 | 过滤 |
| D | 氯化钠溶液 | 碘化钠 | 四氯化碳 | 萃取 |
| A. | A | B. | B | C. | C | D. | D |
| A. | NaCl、NaBr、KI三种无色溶液 | |
| B. | HCl、CaCl2、NaNO3、Na2CO3四种溶液 | |
| C. | NaBr、HCl、KCl三种溶液 | |
| D. | 氯化钠、淀粉碘化钾、溴化钾、溴水四种溶液 |
| A. | C6H6 | B. | C7H8 | C. | C4H10 | D. | C3H6 |
| A. | 向饱和Ca(HCO3)2溶液中加入足量的NaOH溶液:Ca2++HCO${\;}_{3}^{-}$+OH-═CaCO3↓+H2O | |
| B. | 次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO | |
| C. | 1L2mol•L-1的FeBr2溶液中通入2.5mol Cl2:4Fe2++6Br-+5Cl2═10Cl-+4Fe3++3Br2 | |
| D. | 以石墨作电极电解CuCl2溶液:2Cl-+2H2O═2OH-+Cl2↑十H2↑ |
| A. | 75%的酒精用于消毒 | B. | Al(OH)3可用于治疗胃酸过多 | ||
| C. | 明矾用于水的杀菌消毒 | D. | 从海底提取可燃冰 |
 .
. ,空间构型是正四面体,丙烷的结构简式为:CH3CH2CH3异丁烷的结构简式CH3CH(CH3)CH3
,空间构型是正四面体,丙烷的结构简式为:CH3CH2CH3异丁烷的结构简式CH3CH(CH3)CH3