题目内容
【题目】氧、硫位于元素周期表的 VIA 族,其化合物在化工生产中有广泛应用。
(1)CuSO4可由 Cu+H2SO4+H2O2=CuSO4+2H2O 反应制得,该反应应要控制在 40—50℃,原因是________________________________________________。
(2)蛋白质中也含有硫元素,为了测定硫元素质量分数,取蛋白质样品充分燃烧,先用足量碘水吸收二氧化硫,再取吸收液,以淀粉为指示剂,用硫代硫酸钠溶液滴定过量的碘。已知:2S2O32-+I2=S4O62-+2I-
① 滴定终点的现象为:________________________________________。
② 取蛋白质样品 mg 进行测定,采用 C1mol/L 的碘水 V1mL 进行吸收,滴定过量的碘时消耗 C2mol/L 硫代硫酸钠溶液 V2mL。该蛋白质中的硫元素的质量分数为______________。
③ 若燃烧时过量氧气进入吸收液中,可能会导致该蛋白质中的硫元素的质量分数测定值___(填“偏大”或“偏小”或“无影响”)。
(3)苯硫酚(C6H5SH)是一种用途广泛的有机合成中间体。工业上用常用氯苯(C6H5Cl)和硫化氢(H2S)为主要原料制备苯硫酚,但会有副产物苯( C6H6)生成。
I:C6H5Cl(g)+H2S(g) C6H5SH(g)+HCl(g) △H1=-16.8kJ/mol
II:C6H5Cl(g)+H2S(g)===C6H6(g)+ HCl(g)+1/8S8(g) △H2
反应 II 的焓变不易测量,现查表得如下数据:
III: C6H5SH(g)=== C6H6(g)+1/8 S8(g) △H3=-29.0kJ/mol
④ △H2= __________________________
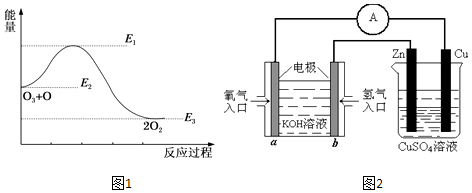
现将一定量的氯苯和硫化氢置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应20分钟测定生成物的浓度,得到图二。
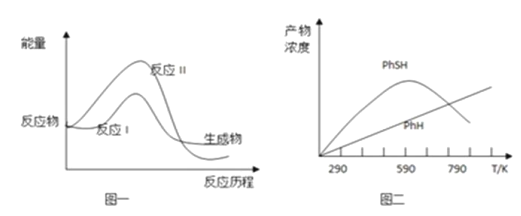
⑤ 上述反应 I、II 的能量变化如图一所示,则在相同条件下,反应速度 v(I)___ v( II)(填写“>”,“<”,“=”)。
⑥ 图二可知,790℃时所测生成物苯硫酚浓度减小,原因为_________
A.温度升高,平衡逆向移动 B.反应Ⅱ温度升高反应速率加快
⑦ 590℃时,2mol 氯苯和 5mol 硫化氢混合气体在 VL 的固定容积中进行反应 I 和II,达到平衡时,测得容器中苯硫酚的物质的量为 1mol,苯的物质的量为0.5mol,则该温度下反应 I 的平衡常数为_______。(保留两位有效数字)
【答案】 温度较低,反应速率慢,温度太高,双氧水分解,损耗大 滴加最后一滴溶液,蓝色恰好褪去,且半分钟不变色 ![]() 偏小 △H2 =45.8 kJ/mol > AB 0.86
偏小 △H2 =45.8 kJ/mol > AB 0.86
【解析】(1)CuSO4可由 Cu+H2SO4+H2O2=CuSO4+2H2O 反应制得,该反应应要控制在 40—50℃,原因是:温度较低,反应速率慢,温度太高,双氧水分解,损耗大。(2)蛋白质样品充分燃烧,先用足量碘水吸收二氧化硫,发生反应:I2+SO2+2H2O=H2SO4+2HI,再取吸收液,以淀粉为指示剂,用硫代硫酸钠溶液滴定过量的碘。发生反应:2S2O32-+I2=S4O62-+2I-① 滴定终点的现象为:滴加最后一滴溶液,蓝色恰好褪去,且半分钟不变色。② 结合反应定量关系计算I2+SO2+2H2O=H2SO4+2HI,2S2O32-+I2═S4O62-+2I-,取蛋白质样品mg进行测定,采用C1mol·L-1的碘水V1 mL进行吸收,滴定过量的碘时消耗C2 mol·L-1硫代硫酸钠溶液V2 mL.与二氧化硫反应的碘单质物质的量n(I2)=n(SO2)=C1V1×10-3mol-C2V2×10-3×1/2mol·L-1,该蛋白质中的硫元素的质量分数=32g·mol-1×(C1V1×10-3-1/2 ×C2V2×10-3)mol/mg×100%=3.2(C1V1-0.5C2V2)/m %;③若燃烧时过量氧气进入吸收液中,氧气也可能氧化二氧化硫,剩余碘的量增大,可能会导致该蛋白质中的硫元素的质量分数测定值偏小。(3)I:C6H5Cl(g)+H2S(g)= C6H5SH(g)+HCl(g) △H1=-16.8kJ/mol、II:C6H5Cl(g)+H2S(g)===C6H6(g)+ HCl(g)+1/8S8(g) △H2,反应 II 的焓变不易测量,现查表得如下数据:III: C6H5SH(g)=== C6H6(g)+1/8 S8(g) △H3=-29.0kJ/mol,④结合盖斯定律计算Ⅰ+Ⅲ得到△H2=-45.8KJ·mol-1;⑤活化能Ⅱ>I,活化能越高,单位体积内活化分子数目越小,反应速率应越慢,故反应速率v(Ⅰ)>v(Ⅱ)。⑥ 图二可知,790℃时所测生成物苯硫酚浓度减小,反应达到平衡状态后升温平衡逆向进行,生成物苯硫酚浓度减小,温度升高反应速率增大,故选AB;⑦590℃时,2mol氯苯和5mol硫化氢混合气体在VL的固定容积中进行反应Ⅰ和Ⅱ,I:C6H5Cl(g)+H2S(g)= C6H5SH(g)+HCl(g) △H1=-16.8kJ/mol
反应量:1 1 1 1
II:C6H5Cl(g)+H2S(g)===C6H6(g)+ HCl(g)+1/8S8(g) △H2
反应量:0.5 0.5 0.5 0.5 0.5
容器中C6H5Cl(g)剩余2mol-1.5mol=0.5mol,H2S(g)剩余5mol-1.5mol=3.5mol,HCl为1.5mol,反应Ⅰ的平衡常数K=生成物平衡浓度幂次方乘积/反应物平衡浓度幂次方乘积,反应前后气体物质的量相同,可以直接用物质的量计算,该温度下反应Ⅰ的平衡常数为K=(1.5×1)/(0.5×3.5)=0.86。

 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案【题目】氯化亚砜(SOCl2)是一种液态化合物,沸点为 77℃,在农药、制药行业中用途广泛。SOCl2遇水剧烈反应,液面上产生白雾,并带有刺激性气味的气体产生.实验室合成原理:SO2+Cl2+SCl2═2SOCl2,部分装置如图所示,(已知 SCl2的沸点为 50℃).
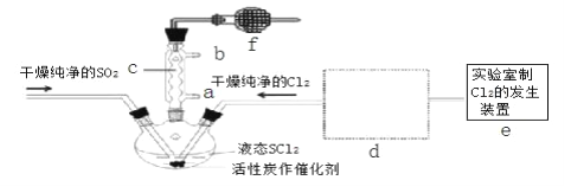
回答以下问题:
(1)下列四种制备 SO2的方案中最佳选择是____________________________
方案 | A | B | C | D |
发生装置 |
|
|
|
|
所选试剂 | 70%H2SO4+K2SO3 | 18.4mol/LH2SO4+Cu | 4mol/LHNO3+Na2SO3 | NaHCO3固体 |
(2)以 MnO2和浓盐酸为原料制备 Cl2的离子方程式为___________________________
(3)仪器 f 的作用是_________________________________________________
(4)d 的虚线框内隐含两个装置,按气流方向顺序这两个装置的药品分别是_______________。
(5)实验结束后,将三颈烧瓶混合物中产品分离出来的方法是 _________________________
(6)若用 SOCl2作 FeCl36H2O 的脱水剂,设计实验证明脱水时发生了氧化还原反应。取少量 FeCl36H2O 于试管中,加入过量 SOCl2,振荡,往试管中加水溶解,滴加____________或________溶液,证明脱水过程发生了氧化还原反应。