题目内容
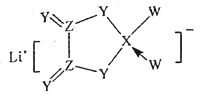
【题目】已知五种短周期元素aX、bY、cZ、dR、eW存在如下关系:① X、Y同主族,R、W同主族 ②![]() ;a+b=
;a+b=![]() (d+e);
(d+e);![]() =c-d,下列有关说法不正确的是
=c-d,下列有关说法不正确的是
A.原子半径比较:r(W)>r(Z)>r(Y) >r(R)
B.X和Y形成的化合物中,阴阳离子的电子层相差1层
C.W的最低价单核阴离子的失电子能力比R的强
D.Z、Y最高价氧化物对应的水化物之间可以相互反应
【答案】A
【解析】
根据R,W 同主族,并且原子序数R为W的一半可知,R为O元素,W为S元素;根据![]() 可知,X和Y的原子序数和为12,又因为X和Y同主族,所以X和Y一个是H元素,一个是Na元素;考虑到
可知,X和Y的原子序数和为12,又因为X和Y同主族,所以X和Y一个是H元素,一个是Na元素;考虑到![]() ,所以X为H元素,Y为Na元素,那么Z为Al元素。
,所以X为H元素,Y为Na元素,那么Z为Al元素。
A.W,Z,Y,R分别对应S,Al,Na,O四种元素,所以半径顺序为:r(Y)>r(Z)>r(W)>r(R),A项错误;
B.X与Y形成的化合物即NaH,H为-1价,H-具有1个电子层,Na为正一价,Na+具有两个电子层,所以,B项正确;
C.W的最低价单核阴离子即S2-,R的即O2-,还原性S2-更强,所以失电子能力更强,C项正确;
D.Z的最高价氧化物对应水化物为Al(OH)3,Y的为NaOH,二者可以反应,D项正确;
答案选A。

【题目】下表是A、B、C、D、E五种有机物的有关信息:
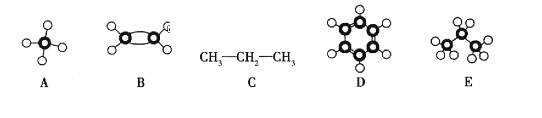
A | B | C | D | E |
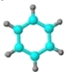
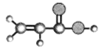
①能使溴的四氯化碳溶液褪色; ②比例模型为: ③能与水在一定条件下反应生成C | ①由C、H两种元素组成; ②球棍模型为: | 分子式为C2H6O,能与E酯化 | ①相对分子质量比C少2; ②能由C氧化而成; | ①由C、H、O三种元素组成; ②球棍模型为: |
根据表中信息回答下列问题:
(1)A到E中,属于烃的是__________(填字母);写出A与溴水反应的化学方程式__________。
(2)B具有的性质是__________(填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水小 ⑤可使酸性高锰酸钾溶液和溴水均褪色
(3)写出C、D 结构简式:__________、__________。
(4)E 中含氧官能团的名称__________。