题目内容
14.常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A.根据题意回答下列问题:(1)H2A为弱酸(填“强”或“弱”).
(2)若溶液M由10mL 2mol•L-1 NaHA溶液与2mol•L-1 NaOH溶液等体积混合而得,则溶液M的pH>7(填“>”、“<”或“=”),原因为A2-+H2O?HA-+OH-(用离子方程式表示),溶液中离子浓度由大到小顺序为c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+).已知Ksp(BaA)=1.8×10-10,向上述混合溶液中加入10mL 1mol•L-1 BaCl2溶液,混合后溶液中的Ba2+浓度为5.4×10-10mol•L-1.
(3)若溶液M有下列三种情况:①0.01mol•L-1的H2A溶液;②0.01mol•L-1的NaHA溶液;③0.02mol•L-1的HCl与0.04mol•L-1的NaHA溶液等体积混合液,则三种情况的溶液中H2A分子浓度最大的为③;pH由大到小的顺序为②>③>①.
(4)若溶液M由pH=3的H2A溶液V1 mL与pH=11的NaOH溶液V2 mL混合反应而得,混合溶液$\frac{c({H}^{+})}{c(O{H}^{-})}$=104,V1与V2的大小关系为均有可能(填“大于”“等于”“小于”或“均有可能”).
分析 (1)存在的分子有H2O、H2A,则H2A为弱酸;
(2)等体积混合生成Na2A,水解显碱性,离子水解以第一步为主;由反应式Ba2++A2-=BaA↓可得:沉淀后A2-过量0.01mol,溶液中c(A2-)=$\frac{0.01mol}{30×1{0}^{-3}L}$=$\frac{1}{3}$mol•L-1,根据BaA的Ksp可得c(Ba2+);
(3)弱酸电离,②中水解生成分子,③中等体积混合为等量的NaCl、NaHA、H2A,浓度均为0.01mol/L,抑制弱酸的电离;
(4)混合溶液c(H+)/c(OH-)=104,c(H+)=10-5mol/L,显酸性,则酸过量,以此分析.
解答 解:(1)存在的分子有H2O、H2A,则H2A为弱酸,故答案为:弱;
(2)等体积混合生成Na2A,水解显碱性,pH>7,离子水解以第一步为主,A2-+H2O?HA-+OH-,则离子浓度关系为c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+),由反应式Ba2++A2-=BaA↓可得:沉淀后A2-过量0.01mol,溶液中c(A2-)=$\frac{0.01mol}{30×1{0}^{-3}L}$=$\frac{1}{3}$mol•L-1,根据BaA的Ksp=c(Ba2+)•c(A2-)可得c(Ba2+)=$\frac{Ksp}{c({A}^{2-})}$=$\frac{1.8{×10}^{-10}}{\frac{1}{3}}$=5.4×10-10 mol•L-1;
故答案为:>;A2-+H2O?HA-+OH-;c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+);5.4×10-10;
(3)弱酸电离,②中水解生成分子,③中等体积混合为等量的NaCl、NaHA、H2A,浓度均为0.01mol/L,抑制弱酸的电离,则三种情况的溶液中H2A分子浓度最大的为③,最小的为②,②溶液pH大于③,①③相比①的酸性强,则pH最小,所以②>③>①,故答案为:③;②>③>①;
(4)混合溶液c(H+)/c(OH-)=104,c(H+)=10-5mol/L,显酸性,则酸过量,H2A为弱酸,pH=3的H2A溶液与pH=11的NaOH溶液混合时酸的浓度大于碱的浓度,则二者体积关系不确定,大于、小于或等于都可能酸过量,故答案为:均有可能.
点评 本题考查较综合,涉及酸碱混合的定性分析、pH、电离与水解、电离方程式等,把握溶液中的溶质及电离与水解的趋势、相互影响即可解答,题目难度中等.

| A. | 氯金酸钠中金元素的化合价为+3 | |
| B. | 葡萄糖具有还原性 | |
| C. | 检测时,NaAuCl4发生氧化反应 | |
| D. | 纳米金单质颗粒分散在水中所得的分散系能产生丁达尔效应 |
| A. | 固体氯化钠不导电,所以氯化钠是非电解质 | |
| B. | 氯化氢水溶液能导电,所以氯化氢是电解质 | |
| C. | 铜丝能导电,所以铜是电解质 | |
| D. | CO2的水溶液能导电,所以CO2是电解质 |
| A. | K+、OH-、CO32 | B. | CO32-、OH-、Cl- | C. | K+、H+、Cl- | D. | Cu2+、H+、Cl- |
| A. | 苯中含有苯酚杂质:加入溴水,过滤 | |
| B. | 乙醇中含有乙酸杂质:加入碳酸钠溶液,分液 | |
| C. | CuCl2溶液中含有FeCl3杂质:加入过量氧化铜粉末,过滤 | |
| D. | CO2中含有HCl杂质:通入饱和Na2CO3溶液,洗气 |
 ,W为( )
,W为( )| A. | CH3CHO | B. | CH3CH2OH | C. | CH3COOH | D. | H2O |
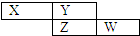 X、Y、Z、W均为短周期元素,它们在周期表的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )| A. | 阴离子的半径从大到小排列顺序为:X>Y>Z>W | |
| B. | X元素的氢化物分子间可以形成氢键 | |
| C. | Y的两种同素异形体在常温下可以相互转化 | |
| D. | 最高价氧化物对应的水化物的酸性:W>Z |