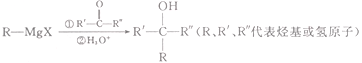题目内容
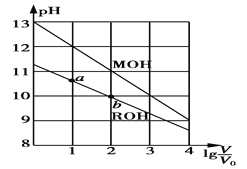
【题目】浓度均为0.10 mol·L-1、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg![]() 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是
A. MOH为弱碱,ROH为强碱
B. ROH的电离程度:a点大于b点
C. 若两溶液无限稀释,则它们的c(OH-)相等
D. 当lg![]() =2时,若两溶液同时升高温度,则
=2时,若两溶液同时升高温度,则![]() 增大
增大
【答案】C
【解析】常温下,0.10 mol·L-1的MOH的PH=13,0.10 mol·L-1的ROH溶液的PH<13,所以MOH为强碱,ROH为弱碱,故A错误;弱电解质越稀电离程度越大,ROH的电离程度:b点大于a点,故B错误;若两溶液无限稀释,最终接近中性,所以它们的c(OH-)相等,故C正确;两溶液同时升高温度,MOH中M+浓度不变,ROH溶液中电离平衡正向移动,R+浓度增大,所以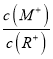 减小,故D错误。
减小,故D错误。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】下列各组微粒能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式书写正确的是( )
选项 | 微粒组(水溶液) | 所加试剂 | 离子方程式 |
A | H+、 Na+、 | Fe粉 | Fe+H+=Fe3++H2↑ |
B | Na+、Cl-、 | 金属钠 | 2Na+2H2O=2Na++2OH-+H2↑ |
C | NH4+、H+、CH3COO- | 氧化铁 | 6H++Fe2O3=2Fe3++3H2O |
D | Ca2+、OH-、Cl- | 通入过量CO2 | OH-+CO2= |
A. A B. B C. C D. D