题目内容
【题目】某化学研究性学习小组模拟工业生产流程制备无水氯化铁并对产物做如下探究实验。
已知:①无水氯化铁在空气中易潮解,加热易升华;
②工业上,向500~600 ℃的铁屑中通人氯气可生产无水氯化铁;
③向炽热的铁屑中通入氯化氢可以生产无水氯化亚铁和氢气,
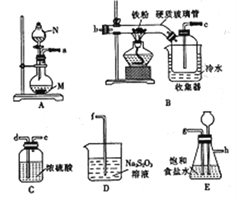
(1)仪器N的名称是____________, N中盛有浓盐酸,烧瓶M中的固体试剂___________(填化学式)。
(2)装置的连接顺序为_______→ → → → → → →d→e→f。(用小写字母表示,部分装置可以重复使用)
(3)若缺少装置E,则对本实验造成的影响是___________________________。
(4)已知硫代硫酸钠(Na2S2O3)溶液在工业上可作脱氯剂,反应后Na2S2O3被氧化为Na2SO4,则装置D中
发生反应的离子方称式为_________________________。
(5)实验结束并冷却后,将硬质玻璃管及收集器中的物质 一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:
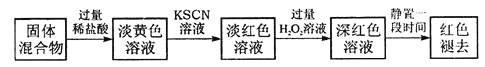
①淡红色溶液中加入过量H2O2溶液后,溶液红色加深的原因是__________________(用离子方程式表示)。
②已知红色褪去的同时有气体生成,经检验气体为O2。该小组对红色褪去的原因进行探究。
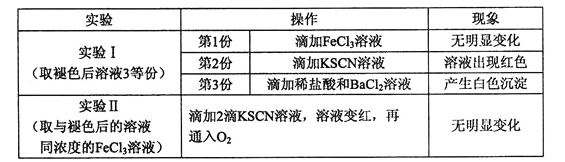
由实验Ⅰ和Ⅱ可得出的结论为____________________。
【答案】 分液漏斗 KMnO4(或KClO3) a,g,h,d,e,b,c HCl和Fe反应生成的H2与Cl2混合受热发生爆炸,且有杂质氯化亚铁生成 S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+(或S2O32-+4Cl2+10OH-=2SO42-+8Cl-+5H2O) 2Fe2++2H++H2O2=2Fe3++2H2O[写作2Fe2++2H++H2O2+6SCN-=2Fe(SCN)2+2H2O也给分] H2O2将SCN-氧化成SO42-
【解析】从题中所给装置来分析,要制备氯化铁得先制备氯气,氯气经净化除去氯化氢和水蒸气后再与铁在加热条件下反应即可制得氯化铁气体,冷凝得氯化铁产品,尾气中有剩余的氯气,要进行尾气吸收处理。
(1). 仪器N的名称是分液漏斗, N中盛有浓盐酸,由于没有酒精灯加热,烧瓶M中的固体试剂必须是常温下能把浓盐酸氧化为氯气的强氧化剂,可以是KMnO4(或KClO3)。
(2). A是氯气发生装置,E是用于除去氯气中的杂质HCl的洗气装置,C要使用两次,一是用于干燥氯气,二是放于B之后防止氯化铁遇水蒸气发生潮解,B是制备氯化铁的装置,D是尾气吸收装置,所以 装置的连接顺序为a→g→h→ d→ e→b→c→d→e→f。
(3). 若缺少装置E,则氯气中的杂质HCl无法除去,由题中信息③可知,向炽热的铁屑中通入氯化氢可以生成杂质无水氯化亚铁,同时生成的H2与Cl2混合受热还有发生爆炸的可能。
(4). 已知硫代硫酸钠(Na2S2O3)溶液在工业上可作脱氯剂,反应后Na2S2O3被氧化为Na2SO4,由此可知氯气将被还原为氯离子,则装置D中
发生反应的离子方称式为S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+(或S2O32-+4Cl2+10OH-=2SO42-+8Cl-+5H2O)。
(5). ①淡红色溶液中加入过量H2O2溶液后,溶液红色加深的原因是在酸性条件下亚铁离子被双氧水氧化为铁离子,铁离子再与硫氰根生成血红色的配合物,这个过程用离子方程式表示为2Fe2++2H++H2O2=2Fe3++2H2O或写成2Fe2++2H++H2O2+6SCN-=2Fe(SCN)2+2H2O。
(6). ②已知红色褪去的同时有气体生成,经检验气体为O2。该小组对红色褪去的原因进行探究。
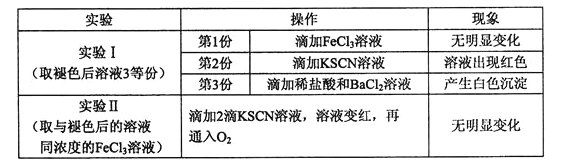
由实验Ⅰ可知,向第1份溶液中加入氯化铁溶液后无明显变化,说明溶液中无SCN-;向第2份溶液中加KSCN溶液后出现红色,说明溶液中有Fe3+;向第3份溶液中滴加盐酸和氯化钡溶液后产生白色沉淀,说明溶液中有SO42-,综合3个实验可得,溶液褪色的原因是SCN-氧化成SO42-。由实验Ⅱ可知,氧气不能将氧化SCN-,由此推理,只能是H2O2将SCN-氧化成SO42-。所以由实验Ⅰ和Ⅱ可得出的结论溶液褪色的原因是H2O2将SCN-氧化成SO42-。

 阅读快车系列答案
阅读快车系列答案【题目】在通风厨中进行下列实验:下列说法不正确的是( )
步骤 |
|
| |
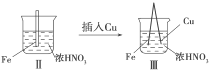
现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
A. Ⅰ中气体由无色变为红棕色的化学方程式:2NO+O2===2NO2
B. Ⅱ中的现象说明Fe表面形成致密的氧化膜,阻止Fe进一步反应
C. 对比Ⅰ、Ⅱ中的现象,说明稀HNO3的氧化性强于浓HNO3
D. 针对Ⅲ中的现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化