题目内容
已知元素R的某种同学素形成离子化和无的化学式为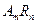 。晶体中一个R微粒的核外电子数为a,核内中子数是b,则该同位素原子的符号是
。晶体中一个R微粒的核外电子数为a,核内中子数是b,则该同位素原子的符号是
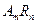 。晶体中一个R微粒的核外电子数为a,核内中子数是b,则该同位素原子的符号是
。晶体中一个R微粒的核外电子数为a,核内中子数是b,则该同位素原子的符号是A.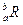 | B.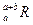 | C.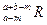 | D.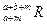 |
C
本题考查原子结构知识;由离子化合物AmRn可知,Rm-的核外电子数为a,则R的质子数为a-m,则其质量数为a-m+n,其原子符号是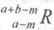 。
。
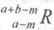 。
。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
题目内容
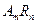 。晶体中一个R微粒的核外电子数为a,核内中子数是b,则该同位素原子的符号是
。晶体中一个R微粒的核外电子数为a,核内中子数是b,则该同位素原子的符号是A.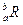 | B.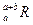 | C.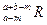 | D.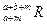 |
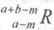 。
。
 阅读快车系列答案
阅读快车系列答案