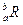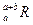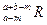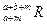题目内容
有X、Y、Z 3种元素,已知X气态氢化物的化学式为H2X,该气态氢化物的式量与X所形成最高价氧化物的式量之比为17∶40,X原子核内质子数与中子数是相同的;Y与X形成离子化合物的化学式为Y2X,Y的阳离子电子层结构与氖相同;Z与X的原子电子层数相同,其气态单质是双原子分子,两原子共用1对电子。
(1)写出各元素的元素符号:X___________,Y___________,Z___________。
(2)X的相对原子质量为___________。
(3)X的离子电子式为___________,X与氢的化合物的电子式为___________。
(4)Y单质在空气中燃烧的化学方程式为______________________。该化合物与水反应的化学方程式为______________________,此反应的离子方程式为______________________。
(5)Z的单质与水反应的化学方程式为_________________________________。
(6)Z2的电子式为___________;Z单质的水溶液与Y2X反应的现象是___________,其化学方程式为(标明电子转移)___________________,此反应的离子方程式为___________________,分析此反应所得到的结论是___________,原因是_____________________。
(1)写出各元素的元素符号:X___________,Y___________,Z___________。
(2)X的相对原子质量为___________。
(3)X的离子电子式为___________,X与氢的化合物的电子式为___________。
(4)Y单质在空气中燃烧的化学方程式为______________________。该化合物与水反应的化学方程式为______________________,此反应的离子方程式为______________________。
(5)Z的单质与水反应的化学方程式为_________________________________。
(6)Z2的电子式为___________;Z单质的水溶液与Y2X反应的现象是___________,其化学方程式为(标明电子转移)___________________,此反应的离子方程式为___________________,分析此反应所得到的结论是___________,原因是_____________________。
(1)S Na Cl
(2)32
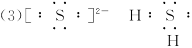
(4)2Na+O2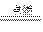 Na2O2 2Na2O2+2H2O====4NaOH+O2↑
Na2O2 2Na2O2+2H2O====4NaOH+O2↑
2Na2O2+2H2O====4Na++4OH-+O2↑
(5)Cl2+H2O====HCl+HClO
(6)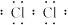 溶液变浑浊
溶液变浑浊
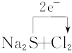 ="===2NaCl+S↓ " S2-+Cl2====S↓+2Cl-
="===2NaCl+S↓ " S2-+Cl2====S↓+2Cl-
Cl2的非金属性比S强(Cl2>S) Cl最外层7e-,S最外层6e-,rCl<rS,Cl得电子能力强
(2)32
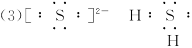
(4)2Na+O2
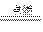 Na2O2 2Na2O2+2H2O====4NaOH+O2↑
Na2O2 2Na2O2+2H2O====4NaOH+O2↑2Na2O2+2H2O====4Na++4OH-+O2↑
(5)Cl2+H2O====HCl+HClO
(6)
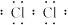 溶液变浑浊
溶液变浑浊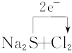 ="===2NaCl+S↓ " S2-+Cl2====S↓+2Cl-
="===2NaCl+S↓ " S2-+Cl2====S↓+2Cl-Cl2的非金属性比S强(Cl2>S) Cl最外层7e-,S最外层6e-,rCl<rS,Cl得电子能力强
已知X的气态氢化物的化学式为H2X,可推得X的最高正价为+6,所以最高价氧化物的化学式应为XO3。又因为H2X与XO3的式量之比为17∶40,即(2+x)∶(x+48)=17∶40,解出x为32。由于X原子核内质子数和中子数相等,所以X为16号硫元素;再根据Y2X可推知Y为+1价,又因为Y的阳离子电子层结构与Ne相同且通过一对共用电子对形成气态双原子分子,可推知Z为氯元素。

练习册系列答案
相关题目
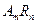 。晶体中一个R微粒的核外电子数为a,核内中子数是b,则该同位素原子的符号是
。晶体中一个R微粒的核外电子数为a,核内中子数是b,则该同位素原子的符号是