题目内容
【题目】常温时,![]() 的
的![]() 和
和![]() 的
的![]() 两种酸溶液,起始时的体积均为
两种酸溶液,起始时的体积均为![]() ,分别向两溶液中加水进行稀释,稀释后溶液体积为V,所得曲线如图所示。下列说法正确的是
,分别向两溶液中加水进行稀释,稀释后溶液体积为V,所得曲线如图所示。下列说法正确的是
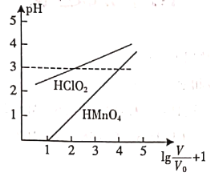
A.在![]() 时,
时,![]() 溶液满足
溶液满足![]()
B.当稀释至pH均为3时,溶液中![]()
C.稀释前分别用![]() 的NaOH溶液中和,消耗的NaOH溶液体积:
的NaOH溶液中和,消耗的NaOH溶液体积:![]()
D.常温下,浓度均为![]() 的
的![]() 和
和![]() 溶液的
溶液的![]()
【答案】A
【解析】
根据图知,lg![]() +1=1时,即溶液未稀释时1mol/L的HMnO4pH=0,说明该溶液中c(H+)=c(HMnO4)=1mol/L,则为HMnO4强酸;lg
+1=1时,即溶液未稀释时1mol/L的HMnO4pH=0,说明该溶液中c(H+)=c(HMnO4)=1mol/L,则为HMnO4强酸;lg![]() +1=1时,1mol/L的HClO2溶液的pH>0,则该酸为弱酸;
+1=1时,1mol/L的HClO2溶液的pH>0,则该酸为弱酸;
A.高锰酸是强酸,完全电离,0≤pH≤5时,稀释多少倍,溶液中c(H+)就是原来的多少分之一,所以HMnO4溶液满足,pH=lg![]() ,故A正确;
,故A正确;
B.根据电荷守恒:c(H+)=c(OH-)+c(ClO2-),c(H+)=c(OH-)+c(MnO4-)当稀释至pH均为3时,c(ClO2-)=c(MnO4-),故B错误;
C.HClO2、HMnO4都是一元酸,中和这两种酸消耗等浓度的NaOH溶液体积与酸的物质的量成正比,两种酸的物质的量浓度相等、体积相等,则两种酸的物质的量相等,所以二者消耗相同物质的量浓度的NaOH体积相等,故C错误;
D.NaMnO4是强酸强碱盐,其水溶液呈中性,NaClO2是强碱弱酸盐,其水溶液呈碱性,所以相同浓度的NaClO2和NaMnO4溶液的pH:NaMnO4<NaClO2,故D错误;
故选:A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目