题目内容
矿石中金的含量很低,金的性质又相当稳定,只能用湿法冶金——氰化法提炼,即采用稀的NaCN溶液处理已粉碎的矿石,把少量的金浸入溶液中,然后用金属锌作还原剂将金从溶液中置换析出。其反应原理为
①4Au+8NaCN+O2+2H2O 4Na[Au(CN)2]+4NaOH;
4Na[Au(CN)2]+4NaOH;
②2Na[Au(CN)2]+Zn 2Au+Na2[Zn(CN)4]。
2Au+Na2[Zn(CN)4]。
以下有关氰化法提炼金的说法中正确的是
①4Au+8NaCN+O2+2H2O
 4Na[Au(CN)2]+4NaOH;
4Na[Au(CN)2]+4NaOH;②2Na[Au(CN)2]+Zn
 2Au+Na2[Zn(CN)4]。
2Au+Na2[Zn(CN)4]。以下有关氰化法提炼金的说法中正确的是
| A.Na[Au(CN)2]不溶于水 |
| B.化合物Na[Au(CN)2]中金元素的化合价为+1 |
| C.金元素在地壳中能以化合态的形式存在 |
| D.在提炼过程中含金元素的物质始终作氧化剂 |
B
试题分析:A、钠盐均是溶于水的,故A错误;B、钠的化合价为+1,C的为+2,N的为-3,故金的化合价为+1,B正确;由方程式①可得在矿石中存在金单质,故C错误;在反应①中金做还原剂,在反应②中含金物质做氧化剂,故D错误;故选B。

练习册系列答案
相关题目



 S
S 

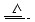 CuSO4+A↑+2H2O
CuSO4+A↑+2H2O