题目内容
(15分)(一)一定温度下,在体积固定的密闭中加入2 mol X和1 mol Y,发生如下反应:2X(g) +
Y(g)  a Z(g) + W(g) △H =-QkJ·mol-1 (Q>0)
a Z(g) + W(g) △H =-QkJ·mol-1 (Q>0)
当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;平衡后再升高温度,混合气体的平均相对分子质量减小,则
(1)温度升高,平衡常数K的值将 (填“增大”.“减小”或“不变”)。
(2)化学计量数a的值为 ,该反应的熵变△S 0(填“>”.“<”或“=”)。
(3)平衡后,若压缩容器体积,则再达到平衡后X的浓度将________(填“增大”、“减少”或“不变”) X的转化率α= (用含Q.Q1的代数式表示)。
(4)维持温度不变,若起始时向容器中加入的物质的量如下列各项,则反应达到平衡后放出的热量仍为Q1 kJ的是 (稀有气体不参与反应)。
A.2 molX.1mol Y.1molAr B.a molZ.1mol W
C.1 molX.0.5mol Y.0.5a molZ.0.5 mol W D.4 molX.2mol Y
(二)若在相同温度下,将2 mol X和1 mol Y加入到容积固定不变的甲容器中,将2amol Z和2 mol W加入到容积可变的乙容器中,t1=5 min时两容器内均达到平衡状态,甲中c(Z)=1.5 mol/L。

请回答下列问题:
(1)5 min内,用X物质表示甲容器中的平均反应速率v(X)=________。
(2)保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙容器中Z的物质的量浓度c(Z)________(填“>”“<”或“=”)3 mol/L。
(3)保持温度不变,t2时分别向甲、乙中加入等质量的氦气后,下图中能表示甲中反应速率变化情况的是________,能表示乙中反应速率变化情况的是________。

(一)(1)减小 (2)1 ,< (3)增大 Q1/Q (4)A
(二) (1)0.6 mol/(L·min) (2) > (3)A C
【解析】(一)(1)正反应放热,所以平衡后再升高温度,平衡向逆反应方向进行,平衡常数减小。
(2)正反应放热,所以平衡后再升高温度,平衡向逆反应方向进行。由于混合气体的平均相对分子质量减小,所以正反应一定是体积减小的,所以熵值是减小的,则a的值为1。
(3)压缩容器体积,则平衡向正反应方向进行,根据勒夏特列原理可知,X的浓度还是增大的。当反应达到平衡后,反应放出的热量为Q1 kJ,则根据热化学方程式可知,消耗X的物质的量是2Q1/Q,所以X的转化率是2Q1/Q÷2=Q1/Q。
(4)这是恒温恒容条件下的等效平衡,即无论如何进行配比,只要把一端按不可逆反应形式完全转化为另一端的物质后,相当于完全等同的起始量即可。所以选项A正确,B和C的状态等效,但放出的热量不是Q1。D中平衡不是等效的,方程式的热量大于2Q1,答案选A。
(二)(1)达到平衡状态,甲中c(Z)=1.5 mol/L,则消耗X是3.0mol/L,所以X的反应速率是3.0mol/L÷5min=0.6 mol/(L·min) 。
(2)反应是体积减小的,则压强也是减小的。所以保持温度不变,移动活塞P,使乙的容积和甲相等时,乙容器中压强是增大的,因此平衡向正反应方向进行,所以Z的浓度大于3.0mol/L。
(3)甲保持容器容积不变,则插入稀有气体,反应速率不变,平衡不移动;乙保持压强不变的,则插入稀有气体,容器容积增大,反应速率降低,平衡向逆反应方向进行,所以正确的答案选A和C。

| ||
(1)该反应中的氧化产物是
(2)800℃下,该反应的平衡常数表达式K=
(3)已知:该反应K800℃>K 850℃,则该反应是
(4)一定温度下,在2L密闭容器内,充入一定量SiO2、C、N2进行上述反应,N2的物质的量随时间(t)的变化如下表:
| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n(N2)/mol | 2.00 | 1.40 | 1.12 | 1.00 | 1.00 | 1.00 |
(5)若压缩(4)中的密闭体系,则上述平衡向
(6)能使SiO2的转化率增大的措施是
A.及时分离出CO气体 B.降低温度 C.增加C的初始量 D.使用适宜催化剂.
(15分)(一)一定温度下,在体积固定的密闭中加入2 mol X和1 mol Y,发生如下反应:2X(g) + Y(g) 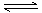 a Z(g) + W(g) △H =-QkJ·mol-1 (Q>0)
a Z(g) + W(g) △H =-QkJ·mol-1 (Q>0)
当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;平衡后再升高温度,混合气体的平均相对分子质量减小,则
(1)温度升高,平衡常数K的值将 (填“增大”.“减小”或“不变”)。
(2)化学计量数a的值为 ,该反应的熵变△S 0(填“>”.“<”或“=”)。
(3)平衡后,若压缩容器体积,则再达到平衡后X的浓度将________(填“增大”、“减少”或“不变”) X的转化率α= (用含Q.Q1的代数式表示)。
(4)维持温度不变,若起始时向容器中加入的物质的量如下列各项,则反应达到平衡后放出的热量仍为Q1 kJ的是 (稀有气体不参与反应)。
| A.2 molX.1mol Y.1molAr | B.a molZ.1mol W |
| C.1 molX.0.5mol Y.0.5a molZ.0.5 mol W | D.4 molX.2mol Y |

请回答下列问题:
(1)5 min内,用X物质表示甲容器中的平均反应速率v(X)=________。
(2)保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙容器中Z的物质的量浓度c(Z)________(填“>”“<”或“=”)3 mol/L。
(3)保持温度不变,t2时分别向甲、乙中加入等质量的氦气后,下图中能表示甲中反应速率变化情况的是________,能表示乙中反应速率变化情况的是________。


 (2009?韶关一模)一定温度下,在密闭容器内进行着某一反应,X气体(2mol)、Y气体(10mol)的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
(2009?韶关一模)一定温度下,在密闭容器内进行着某一反应,X气体(2mol)、Y气体(10mol)的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )