��Ŀ����
��15�֣���һ��һ���¶��£�������̶����ܱ��м���2 mol X��1 mol Y���������·�Ӧ��2X(g) + Y(g) 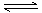 a Z(g) + W(g) ��H =��QkJ��mol��1 (Q>0)
a Z(g) + W(g) ��H =��QkJ��mol��1 (Q>0)
����Ӧ�ﵽƽ���Ӧ�ų�������ΪQ1 kJ������X��ת����Ϊ����ƽ����������¶ȣ���������ƽ����Է���������С����
(1)�¶����ߣ�ƽ�ⳣ��K��ֵ�� (���������С�����䡱)��
(2)��ѧ������a��ֵΪ ���÷�Ӧ���ر��S 0���>������<����=������
(3)ƽ�����ѹ��������������ٴﵽƽ���X��Ũ�Ƚ�________(����������١����䡱) X��ת���ʦ������� (�ú�Q��Q1�Ĵ���ʽ��ʾ)��
(4)ά���¶Ȳ��䣬����ʼʱ�������м�������ʵ��������и����Ӧ�ﵽƽ���ų���������ΪQ1 kJ���� (ϡ�����岻���뷴Ӧ)��
| A��2 molX��1mol Y��1molAr | B��a molZ��1mol W |
| C��1 molX��0.5mol Y��0.5a molZ��0.5 mol W | D��4 molX��2mol Y |

��ش��������⣺
(1)5 min�ڣ���X���ʱ�ʾ�������е�ƽ����Ӧ����v(X)��________��
(2)�����¶Ȳ��䣬�ƶ�����P��ʹ�ҵ��ݻ��ͼ���ȣ��ﵽ�µ�ƽ�����������Z�����ʵ���Ũ��c(Z)________(�>����<������)3 mol/L��
(3)�����¶Ȳ��䣬t2ʱ�ֱ���ס����м���������ĺ�������ͼ���ܱ�ʾ���з�Ӧ���ʱ仯�������________���ܱ�ʾ���з�Ӧ���ʱ仯�������________��

��һ��(1)��С ��2��1 ���� ��3������ Q1��Q ��4��A
������ (1)0.6 mol/(L��min) (2) >��(3)A�� C
����

��ϰ��ϵ�д�
�����Ŀ
�����裨Si3N4����һ�������մɲ��ϣ�800���£�ʯӢ����̿�͵���ͨ�����·�Ӧ���Ƶõ����裮3SiO2��s��+6C��s��+2N2��g��
Si3N4��s��+6CO��g��
��1���÷�Ӧ�е����������� ��
��2��800���£��÷�Ӧ��ƽ�ⳣ������ʽK= ��
��3����֪���÷�ӦK800�棾K 850�棬��÷�Ӧ�� ��Ӧ��������ȡ������ȡ�����
��4��һ���¶��£���2L�ܱ������ڣ�����һ����SiO2��C��N2����������Ӧ��N2�����ʵ�����ʱ�䣨t���ı仯���±���
�ӷ�Ӧ����ƽ��ʱ��CO��ƽ����������Ϊv��CO��= mol/��L?min����
��5����ѹ����4���е��ܱ���ϵ��������ƽ���� ��Ӧ�����ƶ�������������桱����
��6����ʹSiO2��ת��������Ĵ�ʩ�� �������ţ�
A����ʱ�����CO���� B�������¶� C������C�ij�ʼ�� D��ʹ�����˴�����
| ||
��1���÷�Ӧ�е�����������
��2��800���£��÷�Ӧ��ƽ�ⳣ������ʽK=
��3����֪���÷�ӦK800�棾K 850�棬��÷�Ӧ��
��4��һ���¶��£���2L�ܱ������ڣ�����һ����SiO2��C��N2����������Ӧ��N2�����ʵ�����ʱ�䣨t���ı仯���±���
| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n��N2��/mol | 2.00 | 1.40 | 1.12 | 1.00 | 1.00 | 1.00 |
��5����ѹ����4���е��ܱ���ϵ��������ƽ����
��6����ʹSiO2��ת��������Ĵ�ʩ��
A����ʱ�����CO���� B�������¶� C������C�ij�ʼ�� D��ʹ�����˴�����

 ��2009?�ع�һģ��һ���¶��£����ܱ������ڽ�����ijһ��Ӧ��X���壨2mol����Y���壨10mol�������ʵ����淴Ӧʱ��仯��������ͼ��������������ȷ���ǣ�������
��2009?�ع�һģ��һ���¶��£����ܱ������ڽ�����ijһ��Ӧ��X���壨2mol����Y���壨10mol�������ʵ����淴Ӧʱ��仯��������ͼ��������������ȷ���ǣ������� a Z(g) + W(g) ��H =��QkJ��mol��1 (Q>0)
a Z(g) + W(g) ��H =��QkJ��mol��1 (Q>0)
